
在150 ℃时,加热高氯酸铵发生分解反应:2NH4ClO4====N2↑+Cl2↑+2O2↑+4H2O↑,其气态生成物组成的混合气的平均相对分子质量为( )
A.40.75 B.29.375 C.14.69 D.无法计算
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:阅读理解
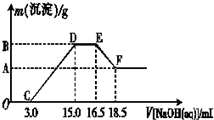 镁、铝、铁及其化合物在生产和生活中有广泛的应用.
镁、铝、铁及其化合物在生产和生活中有广泛的应用.| 实验序号 | I | II | III |
| 加入钢样粉末的质量(g) | 2.812 | 5.624 | 8.436 |
| 生成气体的体积(L)(标准状况) | 1.120 | 2.240 | 2.800 |
| 0.12 |
| 28.12 |
| 0.12 |
| 28.12 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
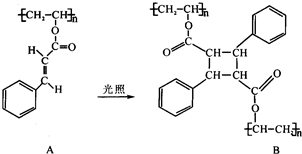 (2011?绵阳模拟)(I)光刻胶是大规模集成电路、印刷电路板和激光刻版技术中的关键材料.某一肉桂酸型光刻胶的主要成分A经光照固化转变为B.
(2011?绵阳模拟)(I)光刻胶是大规模集成电路、印刷电路板和激光刻版技术中的关键材料.某一肉桂酸型光刻胶的主要成分A经光照固化转变为B.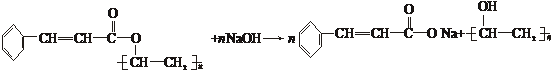
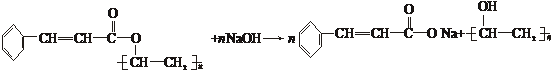
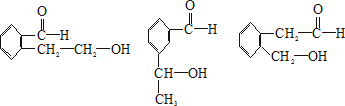

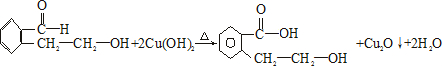

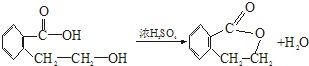
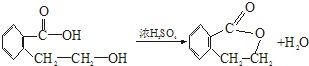
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源:2013届云南省高二上学期期末考试化学试卷 题型:实验题
(4分)下列实验操作不正确的是 (填字母代号)。
A.在催化剂存在的条件下,苯和溴水发生反应可生成无色、比水重的液体溴苯。
B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,完成乙醇氧化为乙醛的实验。
C.醇中含有少量水可加入生石灰再蒸馏制得无水乙醇。
D.试管中先加入一定量浓硫酸,再依次加入冰醋酸、无水乙醇,然后加热制取乙酸乙酯。
E.实验室制取乙烯时,放入几片碎瓷片,以避免混合液在受热沸腾时剧烈跳动。
F.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、待液体分层后,滴加硝酸银溶液。
G.实验室蒸馏石油时温度计水银球插入石油中测量温度,收集60℃~150℃馏分得到汽油。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com