

| A. | 工业上用电解MgCl2溶液的方法冶炼Mg | |
| B. | 钢铁发生吸氧腐蚀的正极反应式为4OH--4e-═O2↑+2H2O | |
| C. | 如图中发生反应的方程式为:Fe+2H+=Fe2++H2↑ | |
| D. | 碱性锌锰干电池放电时的正极反应为:MnO2+H2O+e-=MnOOH+OH- |
分析 A.电解熔融的MgCl2冶炼得到Mg;
B.钢铁发生吸氧腐蚀时正极上氧气得电子生成氢氧根离子;
C.醋酸为弱酸,在离子方程式中要写成分子;
D.碱性锌锰干电池放电时的正极上MnO2得电子生成MnOOH.
解答 解:A.电解熔融的MgCl2冶炼得到Mg,电解MgCl2溶液得到氢氧化镁沉淀,得不到Mg,故A错误;
B.钢铁发生吸氧腐蚀时正极上氧气得电子生成氢氧根离子,则正极上O2+2H2O-4e-═4OH-,故B错误;
C.醋酸为弱酸,在离子方程式中要写成分子,则发生反应的方程式为:Fe+2CH3COOH=Fe2++2CH3COO-+H2↑,故C错误;
D.碱性锌锰干电池放电时的正极上MnO2得电子生成MnOOH,所以正极反应为:MnO2+H2O+e-=MnOOH+OH-,故D正确.
故选D.
点评 本题考查了金属的冶炼、金属的腐蚀、离子方程式的书写、电极方程式的书写等,题目难度不大,侧重于考查学生对电化学原理的应用的考查,注意把握电极方程式的书写和电极的判断.


科目:高中化学 来源: 题型:多选题
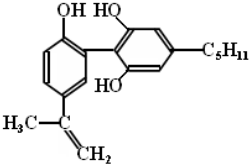
| A. | 该分子中所有碳原子一定都在一个平面上 | |
| B. | 该分子遇FeCl3溶液显紫色,但与苯酚不属于同系物 | |
| C. | 1mol该物质与浓溴水和H2反应时,最多消耗Br2和H2的物质的量分别为4mol、7mol | |
| D. | 滴入酸性KMnO4溶液,观察到紫色褪去,可证明分子中存在双键. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KCl(aq),HCl(aq) | B. | HNO3(aq),KNO3(aq) | C. | HCl(aq),BaCl2(aq) | D. | NaNO3(aq),HNO3(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KClO3+6HCl═3Cl2↑+KCl+3H2O反应中还原剂与氧化剂的物质的量之比为6:1 | |
| B. | 硝酸铵受热分解的化学方程式为:5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O,在反应中被氧化与被还原的氮原子数之比为5:3 | |
| C. | 工业上制备新型净水剂高铁酸钾(K2FeO4)的一步反应如下:2FeCl3+10NaOH+3NaClO═2Na2FeO4+9NaCl+5H2O,若有2 mol FeCl3发生反应,转移电子的物质的量为6 mol | |
| D. | 氮化铝广泛应用于电子陶瓷等工业领域.在一定条件下,AlN可通过反应:Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO合成,方程式中AlN中氮的化合价为-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 . 请回答:
. 请回答: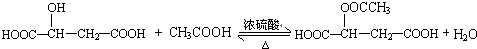 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | I2仅是还原产物 | |
| B. | Cu(IO3)2既是氧化剂又是还原剂 | |
| C. | 氧化产物与还原产物物质的量比为13:2 | |
| D. | 当1 mol氧化剂参加反应时,被氧化的物质的物质的量为11mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CH3CH2CH2-Cl | B. | 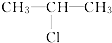 | C. | CH3CH2CH2-Br | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成物所具有的总能量高于反应物所具有的总能量 | |
| B. | 反应物所具有的总能量高于生成物所具有的总能量 | |
| C. | 断开1molH-H键和1molCl-Cl键所吸收的总能量大于形成2molH-Cl键所放出的能量 | |
| D. | 该反应中,化学能只转变为热能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com