
下列说法中错误的是( )
|
| A. | SO2、SO3都是极性分子 |
|
| B. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 |
|
| C. | 元素电负性越大的原子,吸引电子的能力越强 |
|
| D. | PCl3和NF3分子中所有原子的最外层都达到8电子稳定结构 |
考点:
极性分子和非极性分子;原子核外电子排布;元素电离能、电负性的含义及应用;配合物的成键情况.
专题:
原子组成与结构专题.
分析:
A、SO2是极性分子,SO3是非极性分子;
B、存在空轨道和孤对电子的两个微粒之间易形成配位键;
C、元素电负性越大,非金属性就越强,因此吸引电子的能力也越强;
D、在ABn型化合物中,中心元素A的族序数+成键数=8时,满足分子中所有原子都满足最外层8电子结构.
解答:
解:A、中心原子上的价电子都形成共价键的分子为非极性分子,存在孤电子对的分子为极性分子,所以SO2是极性分子,SO3是非极性分子,故A错误;
B、NH4+中N原子中有孤对电子,氢原子有空轨道,形成配位键;[Cu(NH3)4]2+中Cu2+都有空轨道,NH3中N原子有孤对电子,二者形成配位键,故B正确;
C、元素电负性越大,非金属性就越强,因此吸引电子的能力也越强,故C正确;
D、PCl3和NF3分子中,N、P元素都位于第ⅤA族,则5+3=8,满足分子中所有原子都满足最外层8电子结构,故D正确.
故选A.
点评:
本题考查了分子的极性、配位键的判断、电负性、电子式,题目比较简单.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
关于电解NaCl水溶液,下列叙述正确的是( )
|
| A. | 电解时在阳极得到氯气,在阴极得到金属钠 |
|
| B. | 若在阳极附近的溶液中滴入KI溶液,溶液呈棕色 |
|
| C. | 若在阴极附近的溶液中滴入酚酞试液,溶液呈无色 |
|
| D. | 电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
外围电子构型为4d55s1的元素在周期表中的位置是( )
|
| A. | 第4周期第ⅠB族 | B. | 第5周期第ⅠB族 |
|
| C. | 第4周期第ⅥB族 | D. | 第5周期第ⅥB族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
|
| A. | 互为同分异构体的分子结构几乎完全相同 |
|
| B. | 丙氨酸CH3﹣CH(NH2)﹣COOH存在手性异构体 |
|
| C. | 标准状况下,相同体积的NH3、CH4、HF含有相同的电子数 |
|
| D. | 等体积的CO和N2混合后所得的混合气体的平均摩尔质量为28 g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
2008年秋天,毒奶粉事件震惊全国,这主要是奶粉中含有有毒的三聚氰胺.下列关于三聚氰胺分子的说法正确的是( )

|
| A. | 所有碳原子采用sp3杂化,所有氮原子采用sp3杂化 |
|
| B. | 一个分子中共含有15个σ键 |
|
| C. | 属于极性分子,故极易溶于水 |
|
| D. | 分子内既有极性键又有非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
四种元素A、B、C、D,其中A元素原子的原子核内只有一个质子;B的基态原子s能级的总电子数比p能级的总电子数多1;C元素的原子最外层电子数是次外层的3倍; D是形成化合物种类最多的元素.
(1)A、D形成的某种化合物甲是一种重要的化工产品,可用作水果和蔬菜的催熟剂,甲分子中σ键和π键数目之比为 5:1 ;写出由甲制高聚物的反应方程式 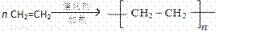 .
.
(2)A、C形成的某种化合物乙分子中含非极性共价键,乙分子属于 (“极性分子”或“非极性分子”);其电子式 ;将乙加入浅绿色酸性溶液中,溶液变为棕黄色,写出该反应的离子方程式.
(3)写出B的基态原子电子排布图为  .与PH3相比,DC2易液化的主要原因是 ;
.与PH3相比,DC2易液化的主要原因是 ;
(4)笑气(B2C)是一种麻醉剂,有关理论认为B2C与CO2分子具有相似的结构.故B2C的空间构型是 ,其为 (填“极性”或“非极性”)分子.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com