
分析 1-丁炔为CH≡C-CH2-CH3,含碳碳三键,与溴以1:2加成;有机物A的分子式与1-丁炔相同,且属于同一类别,则A为CH3C≡CCH3,含碳碳三键,与溴以1:2加成;与1-丁炔互为同系物,且所含碳原子数最少的有机物为乙炔,可发生加聚反应生成高分子化合物.
解答 解:1-丁炔的结构简式为CH≡C-CH2-CH3,含碳碳三键,与溴以1:2加成,则1mol该有机物最多可与2mol溴加成,反应产物的名称是1,1,2,2-四溴丁烷;有机物A的分子式与1-丁炔相同,且属于同一类别,则A为CH3C≡CCH3,含碳碳三键,与溴以1:2加成,与过量溴加成的产物的名称是2,2,3,3-四溴丁烷;与1-丁炔互为同系物,且所含碳原子数最少的有机物为CH≡CH,可发生加聚反应生成高分子化合物聚乙炔,含双键可作导电塑料,
故答案为:CH≡C-CH2-CH3;2;1,1,2,2-四溴丁烷;2,2,3,3-四溴丁烷;CH≡CH;加聚.
点评 本题考查有机物的结构与性质,为高频考点,把握炔烃的结构及性质为解答的关键,注重基础知识的考查,题目难度不大.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | H、D、T互为同素异形体 | |
| B. | 含有共价键的化合物一定是共价化合物 | |
| C. | NH4Cl的电子式: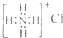 | |
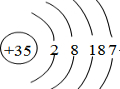
| D. | S2-的结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
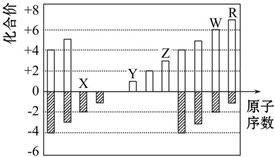
| A. | 原子半径:Z>Y>X | |
| B. | 气态氢化物的稳定性:R<W | |
| C. | WX2和水反应形成的化合物是一种强酸 | |
| D. | Y和Z两者最高价氧化物对应的水化物能相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 事实 | 推测 | |
| A | ${\;}_{12}^{\;}$Mg与水反应缓慢,${\;}_{20}^{\;}$Ca与水反应较快 | ${\;}_{56}^{\;}$Ba(DA族)与水反应会更快 |
| B | 是半导体材料,同族的Ge也是半导体材料 | Ⅳ族的元素都是半导体材料 |
| C | HCl在1500℃时分解,HI在230℃时分解 | HBr的分解温度介于二者之间 |
| D | Si与H2高温时反应,S与H2加热能反应 | P与H2在高温时能反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H | ||||
| 4 | J |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3溶液 | B. | H2SO4溶液 | C. | NaHCO3溶液 | D. | Ba(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| B. | 食品添加剂种类很多,其中的一种为苯甲酸钠,它是苯的一种同系物所对应的钠盐 | |
| C. | 某些蔬菜和水果在人体代谢后,生成碱性物质,所以称为碱性食物 | |
| D. | 抗酸药的种类很多,如碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝、氢氧化镁等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
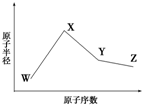 已知W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X、Y、Z同周期,其中X的M层电子数是K层的一半;Y的单质是一种常见的半导体
已知W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X、Y、Z同周期,其中X的M层电子数是K层的一半;Y的单质是一种常见的半导体查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1s22s22p3 | B. | ls22s22p63s23p1 | C. | 1s22s22p2 | D. | 1s22s22p63s23p4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com