
| A. | 丙烯的分子式为:CH3CH=CH2 | B. | H2O2的电子式为: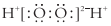 | ||
| C. | S2-的离子结构示意图为: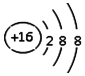 | D. | 苯的比例模型为: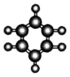 |
分析 A.表示物质的元素组成的式子为分子式;
B.过氧化氢为共价化合物,双氧水中两个氢原子分别与两个氧原子通过共用一对电子结合,两个氧原子之间通过共用1对电子结合;
C.硫离子的核电荷数为16,核外电子总数为18,最外层含有8个电子,据此画出硫离子的离子结构示意图;
D.苯分子中碳碳键为一种介于单键和双键之间的独特键,所有碳碳键完全相同;比例模型能够反映出各原子相对体积大小.
解答 解:A.丙烷的分子式为C3H8,故A错误;
B.双氧水为共价化合物,分子中存在两个氧氢键和一个O-O键,双氧水的电子式为: ,故B错误;
,故B错误;
C.硫离子核外存在18个电子,核内有16个质子,最外层达到8电子稳定结构,其离子结构示意图为 ,故C正确;
,故C正确;
D.苯为平面结构,苯分子中存在6个H和6个C,所有碳碳键完全相同,苯的比例模型为 ,故D错误;
,故D错误;
故选C.
点评 本题考查了离子结构示意图、电子式、分子式的书写,题目难度不大,明确粒子结构示意图的表示方法为解答关键,试题侧重 基础知识的考查,培养了学生的灵活应用能力.


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题

| A. | 原子半径:Z>Y>X. | |
| B. | X和Z形成的化合物能溶于苛性钠溶液 | |
| C. | R元素的含氧酸酸性-定强于W元素的含氧酸的酸性 | |
| D. | Y和W形成的化合物,阴阳离子的个数比可能为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{A}{W+n}$(N-n)mol | B. | $\frac{W}{A+n}$(N+n)mol | C. | $\frac{W}{A+n}$(A-N+n)mol | D. | $\frac{W}{A+n}$(N-A-n)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验编号 | KMnO4溶液的浓(mol/L) | KMnO4溶液滴入的体积(mL) |
| 1 | 0.0200 | V1=20.02 |
| 2 | 0.0200 | V2=23.32 |
| 3 | 0.0200 | V3=19.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷与氯气取代 | B. | 乙烯与氢气加成,再用氯气取代 | ||
| C. | 乙烯与氯化氢加成 | D. | 乙烯与氯气加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
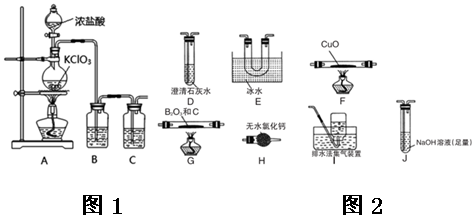
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 滴定次数 实验数据 | 1 | 2 | 3 | 4 |
| 待测溶液体积/mL | 25.00 | 25.00 | 25.00 | 25.00 |
| 滴定管初读数/mL | 0.00 | 0.20 | 0.10 | 0.15 |
| 滴定管末读数/mL | 20.95 | 21.20 | 20.15 | 21.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
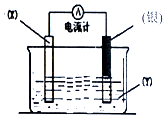 根据氧化还原反应:2Ag++Cu═Cu2++2Ag 设计的原电池如图所示.请回答下列问题:
根据氧化还原反应:2Ag++Cu═Cu2++2Ag 设计的原电池如图所示.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com