
【题目】氨气和氨水在工农业生产中均有重要应用。
(1)工业合成氨反应的化学方程式是_________。
(2)实验室常加热熟石灰[主要成分是Ca(OH)2]和氯化铵混合固体制取氨气,写出反应的化学方程式___________。
(3)如图所示,向表面皿中的NaOH固体滴几滴浓氨水,迅速盖上盖,观察现象。

①___________液滴上方会出现白烟(填序号)
A.浓盐酸 B.浓硫酸 C.FeCl3溶液
②一段时间后浓硫酸的液滴中有白色固体,生成该白色固体的化学方程式是_______。
③FeCl3液滴中出现的现象是___________,发生反应的离子方程式是_________。
(4)利用氨水可以将大气污染物SO2吸收并生产氮肥,原理如图所示:
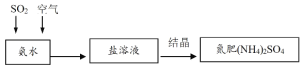
分析上述生产原理,在下列表格中填写该生产过程中利用的SO2的化学性质并进行理论论证
SO2的化学性质 | 理论论证 |
______ | ______ |
______ | ______ |
【答案】N2+3H2 2NH3 Ca(OH)2+2NH4Cl
2NH3 Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O A H2SO4+2NH3=(NH4)2SO4 黄色液滴中产生红褐色沉淀 Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+ 与氨水反应生成铵盐 SO2是酸性氧化物 还原性,被氧气氧化 SO2中S为+4价,可升至+6价,具有还原性,可以与氧气反应生成硫酸盐
CaCl2+2NH3↑+2H2O A H2SO4+2NH3=(NH4)2SO4 黄色液滴中产生红褐色沉淀 Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+ 与氨水反应生成铵盐 SO2是酸性氧化物 还原性,被氧气氧化 SO2中S为+4价,可升至+6价,具有还原性,可以与氧气反应生成硫酸盐
【解析】
(1)工业合成氨,是在高温、高压、并有催化剂作用的条件下,N2与H2反应生成NH3。
(2)熟石灰[主要成分是Ca(OH)2]和氯化铵混合加热,可生成CaCl2和氨气。
(3)氨气与浓盐酸挥发出的HCl气体反应,生成NH4Cl,产生白烟;氨气与浓硫酸反应生成硫酸铵,但看不到明显的现象;氨气与NaOH固体不反应;氨气溶于FeCl3溶液中,生成Fe(OH)3沉淀和NH4Cl。
①由以上分析,可确定哪种液滴上方会出现白烟。
②由以上分析,可确定一段时间后浓硫酸的液滴中白色固体的成分。
③FeCl3液滴中生成Fe(OH)3沉淀。
(4)氨水中通入SO2,发生反应生成(NH4)2SO3;通入空气后,(NH4)2SO3被氧化生成(NH4)2SO4。
(1)工业合成氨,是在高温、高压、并有催化剂作用的条件下,N2与H2反应生成NH3,反应的化学方程式为N2+3H2![]() 2NH3。答案为:N2+3H2
2NH3。答案为:N2+3H2![]() 2NH3;
2NH3;
(2)熟石灰[主要成分是Ca(OH)2]和氯化铵混合加热,可生成CaCl2和氨气,反应的方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O。答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O。答案为:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
(3) ①A.浓盐酸为挥发性酸,挥发出的HCl气体与氨气结合成NH4Cl,产生白烟,A符合题意;
B.浓硫酸为不挥发性酸,与NH3反应生成硫酸铵,但不产生现象,B不合题意;
C.FeCl3溶液与溶解在其中的氨反应,生成红褐色Fe(OH)3沉淀和NH4Cl,C不合题意;
故选A;
②一段时间后浓硫酸的液滴中有白色固体(NH4)2SO4,生成(NH4)2SO4的化学方程式是H2SO4+2NH3=(NH4)2SO4。答案为:H2SO4+2NH3=(NH4)2SO4;
③FeCl3液滴中生成红褐色Fe(OH)3沉淀和NH4Cl,出现的现象是黄色液滴中产生红褐色沉淀,发生反应的离子方程式是Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+。答案为:黄色液滴中产生红褐色沉淀;Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+;
(4)氨水中通入SO2,发生反应生成(NH4)2SO3;通入空气后,(NH4)2SO3被氧化生成(NH4)2SO4。
SO2的化学性质 | 理论论证 |
与氨水反应生成铵盐 | SO2是酸性氧化物 |
还原性,被氧气氧化 | SO2中S为+4价,可升至+6价,具有还原性,可以与氧气反应生成硫酸盐 |
答案为:与氨水反应生成铵盐;SO2是酸性氧化物;还原性,被氧气氧化; SO2中S为+4价,可升至+6价,具有还原性,可以与氧气反应生成硫酸盐。


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,AgCl(s)Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl-)的关系如图所示。下列说法正确的是
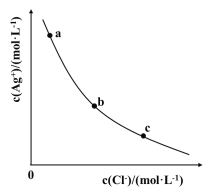
A.a、b、c三点对应的Ksp 不相等
B.AgCl在c点的溶解度比b点的大
C.AgCl溶于水形成的饱和溶液中,c(Ag+)=c(Cl-)
D.b点的溶液中加入AgNO3固体,c(Ag+)沿曲线向c点方向变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示。下列说法正确的是( )
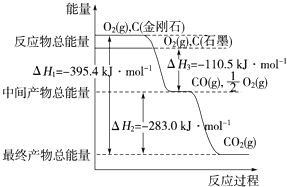
A.等质量的金刚石和石墨完全燃烧,石墨放出的热量更多
B.在通常状况下,金刚石和石墨相比,金刚石更稳定
C.表示石墨燃烧热的热化学方程式为C(石墨,s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
D.36 g石墨转化成金刚石,放出的热量为5.7 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和滴定的误差要求小于0.1%,若用20.00 mL0.2000mol·L-1盐酸滴定20mL0.2000mol·L-1NaOH溶液,则中和滴定曲线中发生突变时的pH范围是(lg2=0.3)( )
A. 4.3~9.7B. 3.7~10.3C. 4.0~10.0D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各溶液中,离子的物质的量浓度关系正确的是
A.pH=4的醋酸中:c(H+)= 0.4mol·L-1
B.饱和碳酸氢钠溶液中(已知碳酸氢钠溶液呈碱性):c(Na+)= c(HCO3-)
C.饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+c(OH-)
D.pH=12的纯碱溶液中:c(OH-)=1.0×10-12mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钒(V)及其化合物有着广泛的用途。请回答下列问题:
(1)钒在溶液中的主要聚合状态与溶液的pH关系如图1所示。V2O74-中V元素的化合价是________,溶液中VO3-转化为V2O74-的离子方程式为________。
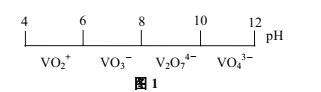
(2)偏钒酸铵是最普通的钒酸盐,将V2O5溶于碳酸钠溶液中(有气体生成),然后加入氯化铵,便可析出偏钒酸铵(NH4VO3),该过程总反应的化学方程式为________;当pH超过8.0时偏钒酸铵会发生转化,其原因是溶液中的VO3-转化为V2O74-、________(请另写出一点原因)。
(3)NH4VO3在高温下分解产生的V2O5可作为硫酸工业中2SO2(g)+O2(g)![]() 2SO3(g)ΔH=pkJ/mol反应的催化剂,其催化原理如图2所示。
2SO3(g)ΔH=pkJ/mol反应的催化剂,其催化原理如图2所示。
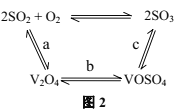
①过程a和过程b的热化学方程式为
V2O5(s)+SO2(g)=V2O4(s)+SO3(g) ΔH=qkJ/mol
V2O4(s)+O2(g)+2SO2(g)=2VOSO4(s) ΔH=rkJ/mol
则过程c的热化学方程式为_________。
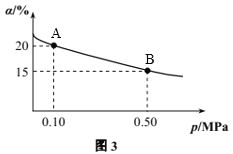
②T℃时反应2SO3(g)![]() 2SO2(g)+O2(g) ΔH>0中SO3的转化率(α)与体系总压强(p)的关系如图3所示。T℃时,将2molSO3置于10L密闭容器中,反应达到平衡后,体系总压强为0.10MPa。则T℃时B点的化学平衡常数Kc=_________。
2SO2(g)+O2(g) ΔH>0中SO3的转化率(α)与体系总压强(p)的关系如图3所示。T℃时,将2molSO3置于10L密闭容器中,反应达到平衡后,体系总压强为0.10MPa。则T℃时B点的化学平衡常数Kc=_________。
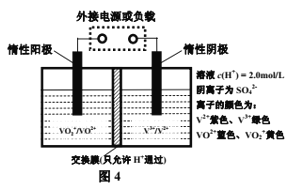
(4)全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图4所示。
①充电过程中,右槽溶液颜色逐渐由________色变为________色;
②充电时若转移的电子数为NA个,则左槽溶液中n(H+)的变化量为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】S2Cl2是橙黄色液体,少量泄漏会产生窒息性气体,喷水雾可减慢其挥发,并产生酸性悬浊液。其分子结构如图所示。下列关于S2Cl2的说法中错误的是( )
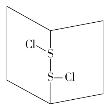
A.S2Cl2为非极性分子
B.分子中既含有极性键又含有非极性键
C.与S2Br2结构相似,熔、沸点S2Br2>S2Cl2
D.与水反应的化学方程式可能为2S2Cl2+2H2O===SO2↑+3S↓+4HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]环丙贝特(H)是一种降血脂药物,可明显降低极低密度和低密度脂蛋白水平,并升高高密度脂蛋白,通过改善胆固醇的分布,可减少CH和LDL在血管壁的沉积,还有溶解纤维蛋白和阻止血小板凝聚作用。如图是合成环丙贝特的一种新方法:
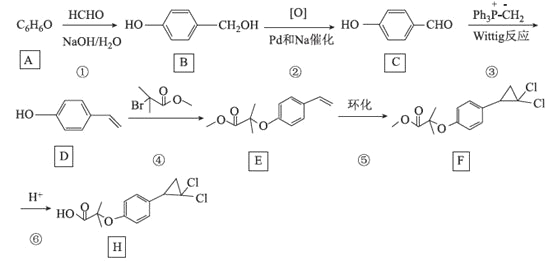
回答下列问题:
(1)C的化学名称为______________________
(2)F中含氧官能团的名称为______________
(3)H的分子式为________________________
(4)反应①的反应类型为___________,反应④的化学方程式为______________________
(5)M为![]() 的同分异构体,能与NaHCO3溶液反应产生气体,则M的结构共有种____(不考虑立体异构);其中1HNMR中有3组峰,且峰面积之比为6:2:1的结构简式为_______
的同分异构体,能与NaHCO3溶液反应产生气体,则M的结构共有种____(不考虑立体异构);其中1HNMR中有3组峰,且峰面积之比为6:2:1的结构简式为_______
(6)利用Wittig反应,设计以环己烷为原料(其他试剂任选),制备![]() 的合成路线:______________________。
的合成路线:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据:
苯 | 溴 | 溴苯 | |
密度/g·cm﹣3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
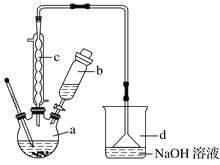
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,是因为生成了_______气体,继续滴加液溴滴完。铁屑的作用是___________;a中发生的化学反应方程式______________________。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是____;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_______;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为______,要进一步提纯,下列操作中必须的是______(填入正确选项前的字母);
A.重结晶B.过滤C.蒸馏D.萃取
(4)在该实验中,a的容积最适合的是_______(填入正确选项前的字母)。
A.25mL B.50mL C.250mL D.500mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com