
下列有关实验的做法不正确的是( )
A.分液时,分液漏斗中的上层液体应由上口倒出
B.用加热分解的方法区分碳酸钠和碳酸氢钠两种固体
C.配制0.100 0 mol·L-1氯化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流
D.检验NH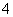 时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体
时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
铁及其化合物与生产、生活关系密切。
(1)下图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
①该电化腐蚀称为________。
②图中A、B、C、D四个区域,生成铁锈最多的是________(填字母)。

(2)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:

①步骤Ⅰ若温度过高,将导致硝酸分解。硝酸分解的化学方程式为______________________________。
②步骤Ⅱ中发生反应:4Fe(NO3)2+O2+(2n+4)H2O===2Fe2O3·nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,该反应的化学方程式为____________________________。
③上述生产流程中,能体现“绿色化学”思想的是______(任写一项)。
(3)已知t ℃时,反应FeO(s)+CO(g)Fe(s)+CO2(g)的平衡常数K=0.25。
①t ℃时,反应达到平衡时n(CO)∶n(CO2)=________。
②若在1 L密闭容器中加入0.02 mol FeO(s),并通入x mol CO, t ℃时反应达到平衡。此时FeO(s)转化率为50%,则x=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
溴及其化合物广泛应用于医药、农药、纤维、塑料组燃剂等,回答下列问题:
(1)海水提溴过程中,向浓缩的海水中通入 ,将其中的Br-氧化,再用空气吹出 溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为 。
溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为 。
(2)溴与氯能以共价键结合形成BrCl。BrCl分子中, 显正电性。BrCl与水发生反应的化学方程式为 。
(3)CuBr2分解的热化学方程式为:
2CuBr2(s)=2 CuBr(s)+ Br2(g) △H=+105.4kJ/mol
在密闭容器中将过量CuBr2于487K下加热分解,平衡时p(Br2)为4.66×103Pa。
①如反应体系的体积不变,提高反应温度,则p(Br2)将会 (填“增大”、“不变”或“减小”)。
②如反应温度不变,将反应体系的体积增加一倍,则p(Br2)的变化范围为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
我国古代“药金”的冶炼方法是:将炉甘石( )和赤铜矿(
)和赤铜矿(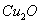 )与木炭按一定的比例混合后加热至800℃,即可炼出闪烁似金子般光泽的“药金”,下列叙述不正确的是( )
)与木炭按一定的比例混合后加热至800℃,即可炼出闪烁似金子般光泽的“药金”,下列叙述不正确的是( )
A、“药金”实质上是铜锌合金
B、冶炼炉中炉甘石直接被碳还原为锌
C、用稀硫酸可区别黄金和“药金”
D、用火焰灼烧不可以区别黄金和“药金”
查看答案和解析>>
科目:高中化学 来源: 题型:
下列描述不符合生产实际的是( )
A.电解熔融的氧化铝制取金属铝,用铁作阳极
B.电解法精炼粗铜,用纯铜作阴极
C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极
D.在镀件上电镀锌,用锌作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验操作或现象中,正确的是( )
A.将新配制的0.1 mol·L-1的NaOH溶液转移到干燥、洁净、带橡胶塞的无色细口瓶中
B.向溶液中通入足量的氯气,以除去Fe2(SO4)3溶液中的FeSO4
C.在中和滴定实验过程中,目光应密切注视滴定管中的液面变化
D.称量NaOH质量时,应在天平的托盘上各放一张纸将NaOH放在纸上
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学课外活动小组,从化学手册上查得硫酸铜在500 ℃以上可以分解成氧化铜、二氧化硫、三氧化硫和氧气,于是设计一验证性实验,探索测定硫酸铜在加热分解时产生的各物质与参加反应的硫酸铜的物质的量的关系。实验用到的仪器如下图所示:
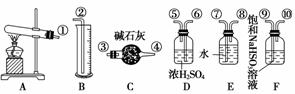
实验测得的数据及有关结果如下:
①准确称取2.4 g无水CuSO4;②干燥管的总质量在实验结束时增加了1.28 g;③测出量筒中水的体积后,折算成标准状况下气体的体积为112 mL。
试回答下列问题。
(1)装置C的作用是________,装置F的作用是________________________。
(2)将装置从左至右连接,各仪器接口的连接顺序为________________________。
(3)反应产生的O2的物质的量为________,SO3的物质的量为____________________。
(4)硫酸铜分解的化学方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子可能大量共存的是
A.不能使酚酞试液变红的无色溶液中:Na+、CO32-、K+、ClO-、AlO2-
B.能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、NH4+
C.pH= 12的溶液中:Na+、Ba2+、NO3-、Cl-
D.无色透明溶液:K+、HCO3-、NO3-、SO42-、Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com