
| A. | 标准状况下,22.4L氯气溶于水转移电子数为NA | |
| B. | 1L 0.1mol/L的硫酸铁溶液中含有铁离子的数目为0.2NA | |
| C. | 向氨气合成塔中通入amolN2和3amolH2的混合气,充分反应后生成N-H数为6aNA | |
| D. | 电解硫酸铜溶液时,当阳极产生22.4L(标况)气体,体系中转移电子数为4NA |
分析 A.氯气与水反应时可逆反应,只有部分氯气与水反应生成氯化氢和次氯酸;
B.Fe3+离子能发生水解;
C.合成氨的反应是可逆反应,反应不能进行到底;
D.电解硫酸铜溶液时,阳极生成的气体为氧气,生成1mol氧气需要得到4mol电子.
解答 解:A.氯气与水反应时可逆反应,只有部分氯气与水反应生成氯化氢和次氯酸,故标准状况下,22.4L氯气溶于水转移电子数小于NA,故A错误;
B.Fe3+离子能发生水解,故1L1mol•L-1硫酸铁溶液中含有Fe3+离子数目小于0.2NA,故B错误;
C.合成氨的反应时可能反应,故氨气合成塔中通入amolN2和3amolH2的混合气,充分反应后生成N-H数小于6NA,故C错误;
D.电解硫酸铜溶液时,阳极产生的气体为氧气,22.4L(标况)气体的物质的量为$\frac{22.4L}{22.4L/mol}$=1mol,生成1mol氧气需要得到4mol电子,电路中转移电子数为4NA,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的应用,难度中等.A为易错点,注意氯气与水的反应中,只有部分氯气与水反应生成氯化氢和次氯酸.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:解答题
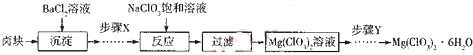
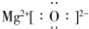 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
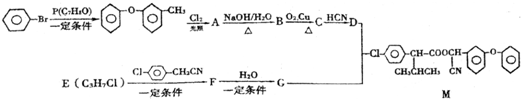
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入足量CO2后的溶液中:Na+、SO32-、CH3COO-、HCO3- | |
| B. | 无色溶液中:Mg2+、MnO4-、SO42-、K+ | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH4+、Fe2+、NO3-、Cl- | |
| D. | c(ClO-)=1.0 mol•L-1的溶液:Na+、SO32-、S2-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海水有“元素故乡”之称,溴被称为“海洋元素” | |
| B. | 发展氯碱工业是利用海水的一大方向,其中氯气是氧化产物,H2是还原产物 | |
| C. | 工业上从海水中获取NaCl和AlCl3,通过电解其熔融盐可获得金属Na和Al | |
| D. | 利用海水通过物理变化可以获得淡水和食盐,但从海水中获取MgCl2和Br2必须通过化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢铁发生吸氧或析氢腐蚀时,铁均作负极被氧化:Fe-3e-═Fe3+ | |
| B. | SO2气体通入Fe2(SO4)3溶液中:SO2+2H2O+2Fe3+═2Fe2++4H++SO42- | |
| C. | 用铜做电极电解CuSO4溶液:2Cu2++2H2O $\frac{\underline{\;电解\;}}{\;}$ 2Cu+O2↑+4H+ | |
| D. | Na2S溶液使酚酞变红:S2-+2H2O?2OH-+H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=1×10-14mol/L的无色溶液:K+、S2-、MnO4-、SO42- | |
| B. | 水电离出的c(H+)=1×10-14mol/L的溶液:K+、Na+、AlO2-、S2O32- | |
| C. | 能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、I- | |
| D. | 能使甲基橙变红的溶液中:Na+、NH4+、Fe2+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16O2与18O2互为同位素,它们的性质基本相同 | |
| B. | 多糖、油脂、蛋白质在一定条件都能发生水解反应 | |
| C. | 玻璃、陶瓷、水泥都是硅酸盐产品,属于无机非金属材料 | |
| D. | 高纯硅广泛应用于太阳能电池、计算机芯片 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.1mol苯分子中含有双键数为0.3NA | |
| B. | 1L1mol•L-1碳酸钠溶液中阴离子的数目大于NA | |
| C. | 标准状况下,22.4L乙烷中共含有分子数为NA | |
| D. | 50mL18.4mol•L-1浓硫酸与足量铜微热反应,转移的电子的数目为0.92NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com