
硼酸(H3BO3)溶液中存在:H3BO3(aq)+H2O(1) [B(OH)4]-(aq)+H+(aq)。下列说法正确的是( )
[B(OH)4]-(aq)+H+(aq)。下列说法正确的是( )
化学式 | 电离常数(298K) |
硼酸 | K=5.7×10-10 |
碳酸 | K1=4.4×10-7 K2=4.7×10-11 |
醋酸 | K=1.75×10-5 |
A.等物质的量浓度的碳酸钠溶液和醋酸钠溶液比较,pH:前者>后者
B.等物质的量浓度的碳酸溶液和硼酸溶液比较,pH:前者>后者
C.将一滴碳酸钠溶液滴入硼酸溶液中一定能观察到有气泡产生
D.将一滴醋酸溶液滴入碳酸溶液中一定能观察到有气泡产生
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源:2016-2017学年吉林长春外国语学校高一上期末理化学卷(解析版) 题型:选择题
下列氯化物可由金属和氯气反应制得,也可由金属与盐酸制得的是( )
A. CuCl2 B. FeCl2 C. FeCl3 D.MgCl2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高一上学期期末化学试卷(解析版) 题型:选择题
将Cu放入0.1 mol•L﹣1FeCl3溶液中,反应一段时间后取出Cu片,溶液中 Fe3+与Fe2+的物质的量浓度之比为4:3,则反应后溶
Fe3+与Fe2+的物质的量浓度之比为4:3,则反应后溶 液中Cu2+与Fe3+的物质的量之比为
液中Cu2+与Fe3+的物质的量之比为
A.3:2 B.3:8 C.4:3 D.3:4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上学期期末化学试卷(解析版) 题型:填空题
食醋的总酸量即一定体积的食醋原液所含醋酸的质量,单位是g· L-1或个g/100mL。国家标准规定酿造食醋总酸含量不得低于3.5g/100mL。
(1)用酸碱滴定法测定某食醋样品中的总酸量时,下列说法中正确的是 。
A.用NaOH溶液滴定时反应的离子方程式为H++OH-=H2O
B.食醋样品不需要预先稀释一定倍数后可以直接进行滴定
C.用NaOH溶液滴定时,可使用酚酞或甲基橙作指示剂
D.若测得样品的物质的量浓度为0.75mol·L-1,则其总酸量为45g·L-1
(2)某同学仔细观察该食醋样品的标签,发现其中还含有作为食品添加剂的苯甲酸钠(C6H5COONa),他想用理论验证醋酸与苯甲酸钠不会发生离子互换反应,需查找在一定温度下醋酸与苯甲酸的 。
A.pH B.电离度 C.电离常数 D.溶解度
(3)常温下,用0.1000mol· L-1 NaOH溶液分别滴定20.00mL 0.1000mol· L-1 HCl溶液和20.00mL 0.1000mol· L-1 CH3COOH溶液,得到两条滴定曲线,如图所示。
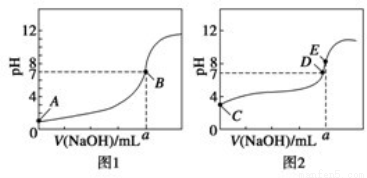
①滴定醋酸溶液的曲线是 (填“图1”或“图2”);滴定曲线中a= mL;
②E点pH>8的原因是(用离子方程式表示): 。
(4)测定食醋的总酸量实验中,配制NaOH溶液和稀释食醋所用的蒸馏水必须煮沸,目的是 。
(5)实验时,吸取食醋样品10mL于100mL容量瓶中定容。移取定容后的溶液20mL于锥形瓶中,加入1~2滴指示剂,用浓度为c mol·L-1的NaOH标准溶液滴定,平行测定三次,消耗NaOH溶液的平均体积为V mL。则原食醋样品的总酸量=____________g/100mL。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上学期期末化学试卷(解析版) 题型:选择题
某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示,下列说法中不正确的是( )

A.b点对应的Ksp等于c点对应的Ksp
B.采取蒸发溶剂的方法可以使溶液从a点变到b点
C.该温度下,Ag2SO4的溶度积常数(Ksp)为1.6×10-5
D.0.02mol·L-1的AgNO3溶液与的0. 2mol·L-1的Na2SO4溶液等体积混合不会生成沉淀
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上学期期末化学试卷(解析版) 题型:选择题
对于aX(g)+bY(g)?cZ(g),为探索外界条件的影响,以X和Y物质的量比为a︰b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如右图所示.以下判断正确的是( )
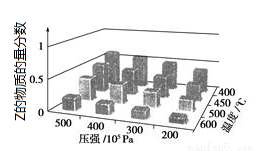
A.△H>0,a+b>c B.△H>0,a+b<c
C.△H<0,a+b>c D.△H<0,a+b<c
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省乐山市高一上学期教学质检化学试卷(解析版) 题型:实验题
实验室配制100 mL 1.0 mol·L-1NaCl溶液有如下操作步骤:
①把称量好的NaCl固体放入小烧杯中,加适量蒸馏水溶解;
②把①所得溶液小心转入容量瓶中;
③将容量瓶塞紧瓶塞,充分摇匀;
④继续向容量瓶中加蒸馏水至液面刻度线下1~2cm处,改用胶头滴管小心滴加蒸馏水至凹液面与刻度线相切;
⑤用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶中,并轻轻摇匀。
请填写下列空白:
(1)计算所需NaCl的质量为 。
(2)操作步骤正确的顺序为 (填序号)。
(3)实验过程中玻璃棒的作用是 ;所需容量瓶的瓶身标有 。
(4)若出现如下情况,分析对所配溶液浓度的影响(填“偏高”、“偏低”或“无影响”):
a. 没有进行操作步骤⑤ ;
b. 开始时容量瓶洗净后没有干燥 ;
c. 定容时俯视容量瓶 。
(5)其实验过程步骤④中加蒸馏水不慎超过了刻度线,应如何处理 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省乐山市高一上学期教学质检化学试卷(解析版) 题型:选择题
下列推断合理的是( )
A.Cu的活动性排在H之后,不能与浓H2SO4发生反应
B.金刚石是自然界中硬度最大的物质,不能氧气发生反应
C.蔗糖中加入浓硫酸后变黑,说明浓硫酸有脱水性
D.将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省等三校高二上第二次联考化学试卷(解析版) 题型:选择题
物质溶于水的过程中通常伴随着能量的变化,下表为四种物质的溶解热(“+”表示吸热,“-”表示放热)。
化学式 | NH4NO3 | NaOH | Ba(NO3)2 | KNO3 |
溶解热(kJ/mol) | +4.13 | -26.01 | + 1.57 | +3.49 |
将等物质的话的上述物质分别加入等质量的水中,所得溶液中水的离子积常数Kw最小的是
A.NH4NO3 B.NaOH C.KNO3 D.Ba(NO3)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com