
科目:高中化学 来源: 题型:选择题
| A. | 钠与水剧烈反应,反应产生的热量导致苯燃烧 | |
| B. | 钠在水层中反应并四处游动,并且发出“啪啪啪”的声音 | |
| C. | 钠在苯的液面上反应并四处游动 | |
| D. | 钠在苯与水的界面处反应并可能作上、下跳动 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将蘸有浓氨水的玻璃棒靠近溶液X | 有白烟产生 | 溶液X是浓盐酸 |
| B | 用玻璃杯蘸取溶液Y进行焰色反应 | 火焰呈黄色 | 溶液Y中含Na+ |
| C | 将Na2SO3固体样品溶液溶解,加入硝酸钡溶液,再加入稀硝酸 | 沉淀不溶解 | Na2SO3样品已变质 |
| D | 向FeSO4溶液中加入硫酸酸化的H2O2溶液 | 溶液变黄 | 氧化性:H2O2>Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
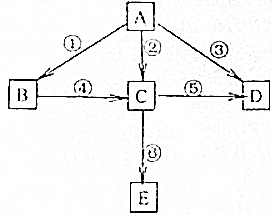 己知A为单质,B、C、D、E为化合物.它们之间存在如图转化关系:
己知A为单质,B、C、D、E为化合物.它们之间存在如图转化关系:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com