

分析 流程分析可知四氯化硅控制温度40°C,加入水水解生成原硅酸和氯化氢,过滤得到盐酸溶液,加入钡矿粉主要成分为BaCO3,且含有铁、镁等离子,调节溶液pH=7,使BaCO3转化为BaCl2,同时使Fe3+完全沉淀,过滤得到滤渣为氢氧化铁,滤液加入氢氧化钠溶液调节溶液pH=12.5,控制70°C,得到氢氧化镁沉淀,过滤得到滤液为氯化钡溶液蒸发浓缩,冷却结晶,过滤洗涤得到氯化钡晶体;
(1)已知:①SiCl4(s)+H2(g)═SiHCl3(s)+HCl(g)△H1=47kJ•mol-1
②SiHCl3(s)+H2(g)═Si(s)+3HCl(g)△H2=189kJ•mol-1
根据盖斯定律,①+②可得;
(2)碳酸钡与盐酸反应生成氯化钡、二氧化碳与水;
(3)滤渣A的主要成分是氢氧化镁、氢氧化钙;温度越高,Ca(OH)2溶解度越小;
(4)蒸发浓缩用到的含硅酸盐的仪器有:蒸发皿、酒精灯、玻璃棒.
解答 解:(1)已知:①SiCl4(s)+H2(g)═SiHCl3(s)+HCl(g)△H1=47kJ•mol-1
②SiHCl3(s)+H2(g)═Si(s)+3HCl(g)△H2=189kJ•mol-1
由盖斯定律,①+②可得:SiCl4(s)+2H2(g)=Si(s)+4HCl(g)△H=+236 kJ•mol-1,
故答案为:SiCl4(s)+2H2(g)=Si(s)+4HCl(g)△H=+236 kJ•mol-1;
(2)碳酸钡与盐酸反应生成氯化钡、二氧化碳与水,反应离子方程式为:BaCO3+2H+=Ba2++CO2↑+H2O,
故答案为:BaCO3+2H+=Ba2++CO2↑+H2O;
(3)滤渣A的主要成分是Mg(OH)2、Ca(OH)2;温度越高,Ca(OH)2溶解度越小,控制温度70℃让钙离子沉淀完全,
故答案为:Mg(OH)2、Ca(OH)2;让钙离子沉淀完全;
(4)蒸发浓缩用到的含硅酸盐的仪器有:蒸发皿、酒精灯、玻璃棒,
故答案为:三.
点评 本题考查物质制备工艺流程,涉及物质的分离提纯、对操作与条件控制分析、热化学方程式书写等,关键是对工艺流程的理解,是对化学实验的综合考查,充分考查了学生的分析理解能力及知识迁移运用的能力,难度中等.


科目:高中化学 来源: 题型:解答题
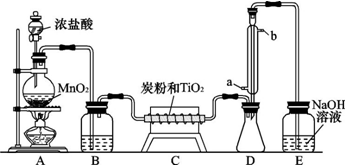
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/K CO2转化率% $\frac{n({H}_{2})}{n(C{O}_{2})}$ | 500 | 600 | 700 | 800 |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
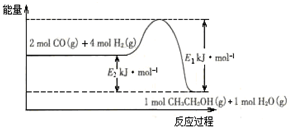
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
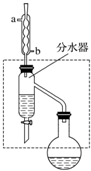 乙酸丁酯是重要的化工原料,具有水果香味.实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:
乙酸丁酯是重要的化工原料,具有水果香味.实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:| 乙酸 | 正丁醇 | 乙酸丁酯 | |
| 熔点/℃ | 16.6 | -89.5 | -73.5 |
| 沸点/℃ | 117.9 | 117 | 126.0 |
| 密度/g•cm-3 | 1.1 | 0.80 | 0.88 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
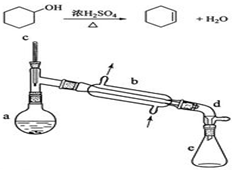 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环已醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环已烯 | 82 | 0.8102 | 83 | 难溶于水 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
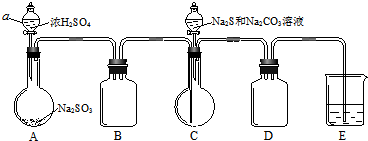
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 | |
| B. | 向水中加入氨水,平衡逆向移动,c(OH-)降低 | |
| C. | 向水中加入金属钠,平衡正向移动,c(H+)增大 | |
| D. | 将水加热,KW增大,pH不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com