
科目:高中化学 来源:不详 题型:填空题
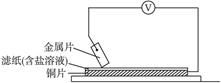
| 金属片 | 电子流动方向 | 电压表读数 |
| A | Cu←A | +0.67 |
| B | Cu→B | -0.71 |
| C | Cu←C | +1.35 |
| D | Cu←D | +0.30 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多 |
| B.同价态的阳离子,甲比乙的氧化性强 |
| C.甲能跟稀盐酸反应放出氢气而乙不能 |
| D.将甲、乙作电极组成原电池时,甲是负极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
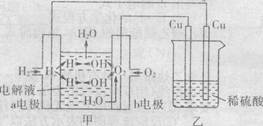
| A.甲是一种具有应用前景的绿色电源 |
| B.甲中b电极的电极反应为:40H-一4e=2H20+02↑ |
C.通电初期乙中的总反应为:Cu + H2SO4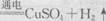 |
| D.反应过程中甲、乙装置的pH都逐渐减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.上述燃料电池的负极反应材料是氢气、甲烷、乙醇等物质 |
| B.氢氧燃料电池常用于航天飞行器,原因之一是该电池的产物为水,经过处理之后可供宇航员使用 |
| C.乙醇燃料电池的电解质常用KOH,该电池的负极反应为:C2H5OH-12e-=2CO2↑+3H2O |
| D.甲烷燃料电池的正极反应为O2+2H2O+4e-=4OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cu Fe FeCl3 |
| B.C Fe Fe(NO3)3 |
| C.Fe Zn Fe2(SO4)3 |
| D.Ag Fe CuSO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
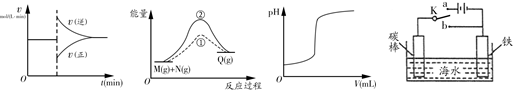
| A.图甲中的曲线可以表示某化学平衡体系改变温度后反应速率随时间的变化 |
| B.图乙中①、②曲线分别表示反应M(g)+N(g)→Q(g)ΔH >0使用和未使用催化剂时,反应过程中的能量变化 |
| C.图丙中的曲线可表示向一定量的氢氧化钠溶液中滴加一定浓度盐酸时的pH变化 |
| D.图丁中开关K置于a或b处均可减缓铁的腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com