
| A. | 氧化银为正极,被还原 | B. | 银为负极,被氧化 | ||
| C. | Zn为负极,被还原 | D. | 该装置中的电解质为酸性物质 |
分析 由充电和放电的反应Ag2O+Zn$?_{充电}^{放电}$2Ag+ZnO可知,放电时为原电池,负极上锌失电子发生氧化反应,正极上氧化银得电子发生还原反应,以此来解答.
解答 解:放电时为原电池,负极上锌失电子发生氧化反应,正极上氧化银得电子发生还原反应,
A.氧化银为正极,被还原,故A正确;
B.负极上Zn失去电子被氧化,发生的反应为:Zn+2OH--2e-═ZnO+H2O,故B错误;
C.Zn为负极,失去电子被氧化,故C错误;
D.Zn及金属氧化物与酸反应,则该装置中的电解质应为碱性物质,故D错误;
故选A.
点评 本题考查原电池知识,为高考常见题型,侧重于学生的分析能力和应用能力的考查,注意把握元素的化合价变化及电极反应式的书写,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验现象 | 实验结论 | |
| A | 将一根未打磨的铝条放入硫酸铜溶液中 | 无紫红色固体析出 | 铝不如铜活泼 |
| B | 将带火星的木条放入氧气瓶中 | 木条复燃 | 氧气能支持燃烧 |
| C | 将CO通过灼热的氧化铜 | 黑色固体变成红色 | CO具有可燃性 |
| D | 将氢氧化钠固体加入水中 | 溶液温度升高 | 该反应是放热反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在化学反应中,反应物转化成生成物,必然发生能量的变化.
在化学反应中,反应物转化成生成物,必然发生能量的变化.| 化学键 | C-H | O-H | C=O | H-H |
| 吸收热量(kJ/mol) | a | b | c | d |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 该电池放电时负极材料是Cd | B. | 该电池放电时是化学能转化为电能 | ||
| C. | 该电池充电时会消耗NiO(OH) | D. | 该电池充电时Cd(OH)2 会失去电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石比石墨稳定 | |
| B. | 1mol 石墨比1mol金刚石的总能量高 | |
| C. | 金刚石和石墨互为同位素 | |
| D. | 石墨比金刚石稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a可能等于b | B. | a一定小于b | C. | a可能大于b | D. | a一定大于b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是酸性氧化物,但不能直接与水反应生成H2SiO3 | |
| B. | N2是大气中的主要成分之一,雷雨时可直接转化为NO2 | |
| C. | 常温下浓硝酸与铝不反应,可用铝制容器存放浓硝酸 | |
| D. | 硅是应用广泛的半导体材料,常温下化学性质活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 两极材料 | Zn片、石墨 | Cu片、Fe片 | Fe片、石墨 | Fe片、Cu片 |
| 插入溶液 | 稀硫酸 | 浓 HNO3 | FeCl3溶液 | 酒精 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第二次月考化学试卷(解析版) 题型:实验题
某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验一 制取氯酸钾和氯水:
利用下图所示的实验装置进行实验。
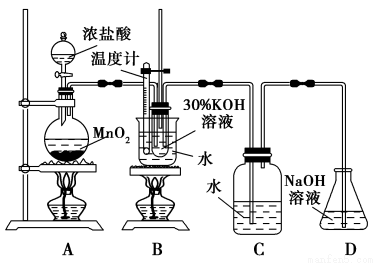
(1)制取实验结束后,取出B中试管冷却结晶、过滤、洗涤。该实验操作过程需要的玻璃仪器有________________。
(2)若对调B和C装置的位置,___________(填“能”或 “不能”)提高B中氯酸钾的产率。
实验二 氯酸钾与碘化钾反应的探究:
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
试管编号 | 1 | 2 | 3 | 4 |
0.20 mol·L-1 KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0 mol·L-1 H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
实验现象 |
①系列a实验的实验目的是______________________。
②设计1号试管实验的作用是_____________________。
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为___________________。
实验三 测定饱和氯水中氯元素的总量:
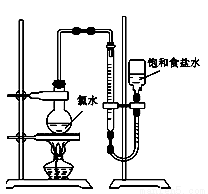
(4)该小组设计的实验方案为:使用如图装置,加热15.0 mL饱和氯水试样,测定产生气体的体积。此方案不可行的主要原因是_____________。(不考虑实验装置及操作失误导致不可行的原因)
(5)根据下列资料,为该小组设计一个可行的实验方案(不必描述操作过程的细节): _____________________。
资料:i.次氯酸会破坏酸碱指示剂;ii.次氯酸或氯气可被SO2、H2O2、FeCl2等物质还原成Cl-。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com