
分析 (1)Na2FeO4在水溶液中阴离子水解平衡移动的影响因素结合实际应用来判断;
(2)由反应信息知道:反应物是金属锌、高铁酸钠,产物是氢氧化铁、氢氧化锌,据此来书写方程式;
(3)已知n(NO)=$\frac{2.688L}{22.4L/mol}$=0.12mol,溶液中还有H+,说明硝酸未反应完,所以溶液中只含Fe3+,根据N元素守恒计算n(NO3-),根据电荷守恒计算n(Fe3+),再根据固体的质量计算.
解答 解:(1)Na2FeO4在水溶液中会发生水解,并且水解后溶液呈碱性,如果在氢氧化钠溶液中,NaOH溶液呈碱性,会抑制其水解,有利于减少产品损失,
故答案为:Na2FeO4 在水溶液中水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解,有利于减少产品损失;
(2)根据反应信息知道:反应物是金属锌、高铁酸钠、产物是氢氧化铁、氢氧化锌,配平后的方程式为3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH,
故答案为:3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH;
(3)n(NO)=$\frac{2.688L}{22.4L/mol}$=0.12mol,溶液中还有H+,说明硝酸未反应完,所以溶液中只含Fe3+,溶液中有n(NO3-)=0.2L×4mol•L-1-0.12mol=0.68mol,根据电荷守恒 n(NO3-)×1=n(H+)×1+n(Fe3+)×3,n(Fe3+)=0.2mol,样品中所有铁元素物质的量为0.2mol.
设样品中Fe的物质的量为x,Fe3O4的物质的量为y
56g•mol-1×x+232g•mol-1×y=13.12g
x+3y=0.2mol,
解得:x=0.11mol,y=0.03mol
单质铁的质量分数为$\frac{0.11mol×56g/mol}{13.12g}$=0.47,
答:该黑色粉末中Fe的质量分数0.47.
点评 本题综合考查学生盐的水解原理以及应用、原电池的工作原理以及元素以及化合物性质的计算等知识,属于综合知识的考查,难度中等,侧重于考查学生的分析能力和计算能力.


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 铁原子的质量数均为60 | |
| B. | ${\;}_{26}^{60}$Fe的核内质子数比中子数多8 | |
| C. | 1mol${\;}_{26}^{58}$Fe与足量盐酸反应时均可得到1mol H2 | |
| D. | 等物质的量的${\;}_{26}^{60}$Fe与1mol ${\;}_{26}^{58}$Fe,前者质量比后者多2g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
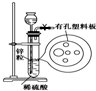 如图为实验室制氢气的简易装置.若在加稀硫酸时发现锌粒与稀硫酸没有接触而稀硫酸不够了,为使该反应顺利进行,可以从长颈漏斗中加入的试剂是( )
如图为实验室制氢气的简易装置.若在加稀硫酸时发现锌粒与稀硫酸没有接触而稀硫酸不够了,为使该反应顺利进行,可以从长颈漏斗中加入的试剂是( )| A. | ①③⑤ | B. | ①②③ | C. | ④⑤⑥ | D. | ①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
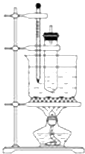 苯与浓硝酸的反应:实验室制备硝基苯的实验装置如下图所示,主要步骤如下:
苯与浓硝酸的反应:实验室制备硝基苯的实验装置如下图所示,主要步骤如下: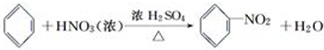 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,23gNO2含有NA个氧原子 | |
| B. | 常温常压下,18mLH2O约含有NA个H2O分子 | |
| C. | 含14 NA个电子的N2分子的物质的量是1mol | |
| D. | 0.1mol/L的Ba(OH)2溶液中,OH-的个数为0.2NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

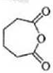 .
.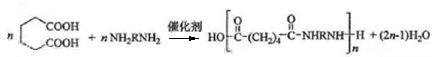 .
.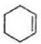 $\stackrel{溴的四氯化碳溶液}{→}$
$\stackrel{溴的四氯化碳溶液}{→}$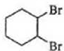 $→_{△}^{氢氧化钠/醇}$
$→_{△}^{氢氧化钠/醇}$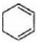 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
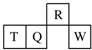 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 原子半径:T>Q>R | |
| D. | T的非金属性强于Q的非金属性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
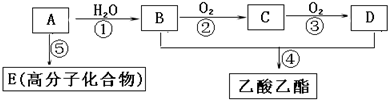
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com