
����Ŀ����������;�㷺�Ļ���ԭ�ϣ�������ˮ������ˮ�����������ʹ����ȡ�
(1)��ϡ���ᡢͭ����������ȡ����ͭ����������Ҫ��������ͼ��ʾ��

ϡ���ᡢͭ����������Ӧ�������漰���ķ�Ӧ�����ӷ���ʽ��______________��������Һ��ͨ���ȿ����ķ�Ӧ�����ӷ���ʽ��__________������Һ�õ���ˮ����ͭ��ʵ�������________��
(2)�������������������Ṥҵβ���еĶ�������ͬʱ�Ƶ�����泥���Ҫ�Ĺ�����������ͼ��ʾ��

���������з�����Ӧ�Ļ�ѧ����ʽ��______________________��
�������ݱ���������������Һ��pH��5.5��6.0֮�䣬����Ч�ʽϸߣ�������һ��������β��ʱ��������Һ��pH�ķ�����______��
���𰸡�Fe2O3+6H+=2Fe3++3H2O��2Fe3++Cu=2Fe2++Cu2+ 4Fe2++4H++O2=4Fe3++2H2O �����ᾧ��������ˮ 4NH3H2O+2SO2+O2=2(NH4)2SO4+2H2O ���ڰ�ˮ������������
��������
(1)�����������ᷴӦ��������������������ͭ��Ӧ��������ͭ�����������������й����ȵĿ�������Fe2+����ΪFe3+������Cu(OH)2CO3��������Һ��pH=4����Ӧ�������ɫFe(OH)3���������������˳��������ȣ��õ�����Fe2O3����Һ��CuSO4��
(2)���������Ṥҵβ���еĶ�������ͬʱ�Ƶ�����泥���������ͨ�����������������������������Ϊ�����Σ�
������������Һ��pH��5.5��6.0֮�䣬����Ч�ʽϸߡ�������һ��������β��ʱ��������Һ��pH�ķ����ǿ��ư�����������
(1)��������ת��ͼ�����������������ᷴӦ��������������������ͭ��Ӧ��������ͭ��������������Ӧ�����ӷ���ʽΪ��Fe2O3+6H+=2Fe3++3H2O��2Fe3++Cu=2Fe2++Cu2+����ͨ�����������Fe2+ΪFe3+�����ӷ���ʽΪ��4Fe2++4H++O2=4Fe3++2H2O������Cu(OH)2CO3��������ҺpH=4��Fe3+�γ�Fe(OH)3������ȥ���õ�����ͭ��Һ����������Ũ���ᾧ�õ�����ͭ���壬�����������ˮ�õ���ˮ����ͭ��
(2)����������ͼ�������������з�����Ӧ�Ƕ�������һˮ�ϰ���������Ӧ��������狀�ˮ����Ӧ�Ļ�ѧ����ʽΪ��4NH3H2O+2SO2+O2=2(NH4)2SO4+2H2O��
������������Һ��pH��5.5��6.0֮�䣬����Ч�ʽϸߣ�������һ��������β��ʱ����ͨ�����ڰ�ˮ��������������������Һ��pH��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������º�̼����H2CO3��HCO3����CO32��������CO2��NaOH��Һ��Ӧ�����Һ�У����ǵ����ʵ�����������ҺpH�Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� ��
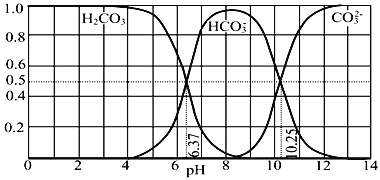
A. Ϊ��þ����ܴ���NaHCO3���˿�����Һ��pHΪ7��9֮��
B. pH=10.25ʱ��c(Na+)=c(CO32��)+c(HCO3��)
C. ����ͼ�����ݣ����Լ���õ�H2CO3��һ�������ƽ�ⳣ��K1(H2CO3)=10��6.37
D. ����0.1mol NaOH��Ӧ�����õ�1L��Һ��pH=10ʱ����Һ�д������¹�ϵ�� c(Na+)��c(HCO3��)��c(CO32��)��c(OH��)��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�����ӿ�ʼ���ڹر�״̬����Һ��A�����Թܢ�������B��ַ�Ӧ�����ӣ��ɷ����Թܢ��ڵ�ˮ���̷����ˡ�Һ��A������B������������ǣ� ��

A. ����������Һ��һ������
B. ˮ������
C. ����������Һ��������̼
D. ˮ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¶Ⱥ�ѹǿ��ͬʱ���������ͬ�������ܱ��������ң����г���O2���壬���г���O2��O3�Ļ�����壬����˵����ȷ����
A. �������������������� B. ������������ķ�����Ŀ���
C. ���������������ԭ����Ŀ��� D. ��������������ܶ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijϡ�����ϡ����Ļ����Һ200 mL��ƽ���ֳ����ݣ�������һ��������ͭ�ۣ�������ܽ�19.2 g(��֪����ֻ�ܱ���ԭΪNO����)������һ�����������ۣ�������������������������ӵı仯��ͼ��ʾ�����з��������������(����)

A. �����Һ��NO3-�����ʵ���Ϊ0.4 mol
B. OA�β�����NO��AB�η�ӦΪ2Fe3��+Fe=3Fe2����BC�β�������
C. ��Һ����������ΪFeSO4
D. c(H2SO4)Ϊ5 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ƻ������ǽ�ú�е���Ԫ����CaSO4����ʽ�̶�����ú̿ȼ�չ����в�����CO�ֻᷢ����ӦI�ͷ�ӦII����������Ч�ʽ��͡�ij�¶��£���ӦI������(v1)���ڷ�ӦII������(v2)�������з�Ӧ���������仯ʾ��ͼ��ȷ����
��ӦI��CaSO4(s)+CO(g) ![]() CaO(s)+SO2(g)+CO2(g) ��H1=+218.4kJ��mol-1
CaO(s)+SO2(g)+CO2(g) ��H1=+218.4kJ��mol-1
��ӦII��CaSO4(s)+4CO(g) ![]() CaS(s)+4CO2(g) ��H2=��175.6kJ��mol-1
CaS(s)+4CO2(g) ��H2=��175.6kJ��mol-1
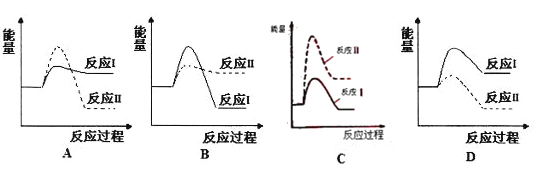
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о���������ʴ�����з�������ȷ����
��� | �� | �� | �� |
ʵ�� |
|
|
|
���� | 8Сʱδ�۲� ��������ʴ | 8Сʱδ�۲� ��������ʴ | 1Сʱ�۲� ��������ʴ |
A. ���У�NaCl��Һ���ܽ��O2������ʹ����Ƭ������ʴ
B. ���У�����Ƭδ������ʴ��ԭ��֮һ��ȱ��H2O
C. ����������Ӧ��O2+4e+ 2H2O ==4OH
D. �ԱȢ٢ڢۣ�˵�����ܸ���O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鲻��������
A. ֤���ǽ�����ǿ�� S��C��Si 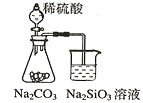
B. ���Ȼ�̼��ȡ��ˮ�еĵ�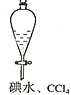
C. �Ʊ����ռ�����NO����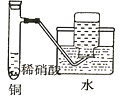
D. �Ʊ���������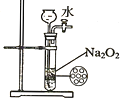
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о���Ӧ��Ļ�ѧ�����������֮��Ĺ�ϵʱ��ʹ����������ķ��������յ�ֱ�������Ч�������б��ﲻ��ȷ����(����)
A. NaOH��Һ��SO2��Ӧʱ��Һ�����ʵ���� ![]()
B. NaAlO2��Һ�����ᷴӦ�����Ĵ�����ʽ![]()
C. Fe��Cl2��ȼ�ղ���![]()
D. Fe��ϡ���ᷴӦ�����Ĵ�����ʽ![]()
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com