
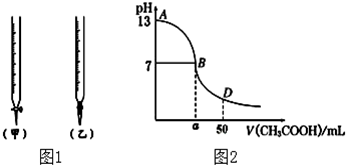
| 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
| A | 碱 | 酸 | 石蕊 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 酚酞 | (甲) |
| D | 酸 | 碱 | 石蕊 | (乙) |
| 待测氢氧化钠 | 0.100mol/L醋酸的体积 | ||
| 滴定次数 | 溶液的体积(mL) | 滴定前的刻度(mL) | 滴定后的刻度(mL) |
| 第一次 | 25.00 | 0.00 | 24.98 |
| 第二次 | 25.00 | 1.56 | 27.86 |
| 第三次 | 25.00 | 0.22 | 25.24 |
| c(标准)V(标准) |
| V(待测) |
| c(标准)V(标准) |
| V(待测) |
| c(标准)V(标准) |
| V(待测) |
| c(标准)V(标准) |
| V(待测) |
| c(标准)V(标准) |
| V(待测) |
| 24.98+26.30+25.02 |
| 3 |
| 25.43mL×0.1000mol/L |
| 25mL |


科目:高中化学 来源: 题型:
| A、导致易拉罐变瘪的反应是:CO2+2OH-=CO32-+H2O |
| B、导致易拉罐又鼓起来的反应是:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
| C、取易拉罐内反应后的溶液,逐滴加入足量的盐酸,只能发生3个化学反应 |
| D、如果将CO2换为NH3,浓NaOH溶液换为浓盐酸,易拉罐也会出现先瘪后鼓的现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol的白磷(P4)或四氯化碳(CCl4)中所含的共价键数均为0.4NA |
| B、1L amol/L的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目为3NA |
| C、0.1 molN2和0.3molH2在一定条件下充分反应,转移电子数目为0.6NA |
| D、常温常压下,65gZn与足量浓 H2SO4充分反应,转移电子数一定为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升温增压 | B、降温减压 |
| C、升温减压 | D、降温增压 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol?L-1) | 0.64 | 0.50 | 0.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、工作一段时间后,C烧杯的PH减小 |
| B、电极I发生还原反应 |
| C、盐桥中的K+移向A烧杯 |
D、电流方向:电极Ⅳ→ →电极I →电极I |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、阿司匹林具有解热镇痛作用 |
| B、可以用Si3N4、Al2O3制作高温结构陶瓷制品 |
| C、禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染 |
| D、在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
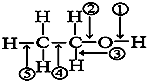
| A、和金属钠作用时,键①断裂 |
| B、和浓硫酸共热至170℃时,键②和⑤断裂 |
| C、和乙酸、浓硫酸共热时,键②断裂 |
| D、在银催化下和氧气反应时,键①和③断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、光导纤维、硝化纤维、铜氨纤维、玻璃纤维的主成分都是糖类 |
| B、生理盐水、葡萄糖注射液都不能产生丁达尔效应现象,不属于胶体 |
| C、红外光谱仪可用于测定化合物的官能团、1H核磁共振仪可确定H所处的化学环境 |
| D、用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可到达水果保鲜的目的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com