
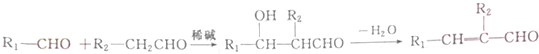

 ��GΪCH3CH=CHCHO����һ�����η��Ƶ�CΪ
��GΪCH3CH=CHCHO����һ�����η��Ƶ�CΪ ��BΪ
��BΪ ��AΪ
��AΪ ��FΪCH3CH��OH��CH2CHO��EΪCH3CHO���ݴ˴��⣮
��FΪCH3CH��OH��CH2CHO��EΪCH3CHO���ݴ˴��⣮ ��GΪCH3CH=CHCHO����һ�����η��Ƶ�CΪ
��GΪCH3CH=CHCHO����һ�����η��Ƶ�CΪ ��BΪ
��BΪ ��AΪ
��AΪ ��FΪCH3CH��OH��CH2CHO��EΪCH3CHO��
��FΪCH3CH��OH��CH2CHO��EΪCH3CHO�� +O2
+O2| Cu |
| �� |
 +2H2O��
+2H2O�� +O2
+O2| Cu |
| �� |
 +2H2O��
+2H2O�� 


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ͭ����ϡ���Cu+2H++NO3-=Cu2++NO2��+H2O | ||
| B����KIO3����������Һ�е�KI��5I-+IO3-+3H2O=3I2+6OH- | ||
| C����NaAlO2��Һ��ͨ�������CO2��2AlO2-+CO2+3H2O=2Al��OH��3��+CO32- | ||
D��������Cu��OH��2����Һ�м�����ȩ��Һ�����ȣ�CH3CHO+2Cu��OH��2+OH-
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���ĵ��壮ij���������л���A������ʽC4H9Br����������3�������ͼ״�Ϊ�л�ԭ�Ϻϳ�H���ϳ�·�����£�
���ĵ��壮ij���������л���A������ʽC4H9Br����������3�������ͼ״�Ϊ�л�ԭ�Ϻϳ�H���ϳ�·�����£�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2.24L H2O������� |
| B��22g CO2 |
| C��9.03��1023��O2 |
| D��2mol H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
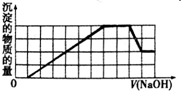 ij��Һ�п��ܺ���H+��NH4+��Fe3+��Al3+��SO42-��CO32-�����ӣ��������Һ�м���һ�����ʵ���Ũ�ȵ�NaOH��Һʱ���������ɳ��������ʵ�����NaOH��Һ������仯��ͼ����ͼ��ʾ������˵����ȷ���ǣ�������
ij��Һ�п��ܺ���H+��NH4+��Fe3+��Al3+��SO42-��CO32-�����ӣ��������Һ�м���һ�����ʵ���Ũ�ȵ�NaOH��Һʱ���������ɳ��������ʵ�����NaOH��Һ������仯��ͼ����ͼ��ʾ������˵����ȷ���ǣ�������| A��ԭ��Һ�к��е�������ֻ��H+��Fe3+��Al3+ |
| B��ԭ��Һ��һ������SO42-��Na+ |
| C��ԭ��Һ�к��е�Fe3+��Al3+�����ʵ���֮��Ϊl��l |
| D����Ӧ����γɵ���Һ������ֻ��Na2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����H3=2��H1-��H2 |
| B����H3=��H1+��H2 |
| C����H3=2��H1+��H2 |
| D����H3=��H2-��H1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ת����Һ��δϴ���ձ��Ͳ�������ֱ�Ӷ��� |
| B��������ƿ�н��ж���ʱ���ӿ̶��� |
| C��������ƿ�н��ж���ʱ���ӿ̶��� |
| D�����ݺ������ƿ��תҡ�ȣ�����Һ����ڿ̶ȣ��ٲ��伸��ˮ���̶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���Ȼ�����Һ | B��NaOH��Һ |
| C����̪��Һ | D������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com