
在盛有足量A的体积可变的密闭容器中通入B,发生反应:A(s)+ 2B(g) 4C(g)+ D(g)△H>0,在一定温度、压强下达到平衡。平衡时C的物质的量与通入B的物质的量的变化关系如图所示。下列说法正确的是:( )
4C(g)+ D(g)△H>0,在一定温度、压强下达到平衡。平衡时C的物质的量与通入B的物质的量的变化关系如图所示。下列说法正确的是:( )
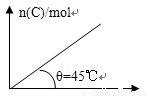
A.平衡时B的转化率为20%
B.若再通入B,则再次达平衡时C的体积分数增大
C.在容器中加入催化剂,则B的转化率增大
D.若保持压强一定,当温度升高时,图中θ>45°
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源:2015-2016学年浙江省宁波市高一下学期学考期中化学试卷(解析版) 题型:选择题
l体积某气态烃完全燃烧需消耗相同条仵下3体积O2,该气态烃是
A. CH4 B.C2H2 C.C2H4 D.C3H6
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省宁波市高二下学期期中考试化学试卷(解析版) 题型:选择题
将CO2气体缓缓通入到含有等物质的量的KOH、Ba(OH)2和KAlO2的混合溶液中,直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示(假设每步反应均完全)。下列关于整个反应进程中的各种描述不正确的是
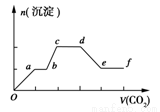
A.a~b段与c~d段所发生的反应相同
B.b~c段反应的离子方程式是:
2Al O2-+3H2O+CO2===2Al(OH)3↓+C O32?
C.O~a段反应的化学方程式是:Ba(OH)2+CO2===BaCO3↓+H2O
D.d~e段沉淀的减少是由碳酸钡固体的消失所致
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省宁波市高二下学期期中考试化学试卷(解析版) 题型:选择题
某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生。下列化合物中符合上述条件的是
A.AlCl3 B.Na2O C.FeCl2 D.SiO2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下学期期中考试化学试卷(解析版) 题型:推断题
已知A、B、C、D、E五种短周期主族元素的原子序数依次增大,A是元素周期表中原子半径最小的,C与A同主族;A与B、D、E所形成的常见化合物在常温下均呈气态,在周期表中D与E左右相邻,B的最高价氧化物的水化物与其氢化物反应生成盐,且B的核电荷数与E的最外层电子数相同。请回答下列问题:
(1)C的离子结构示意图是 。
(2)A、B、E可组成一种化合物,其原子个数之比为4:1:1,该化合物中存在的化学键类型 。
(3)D2E2分子的结构式为 ;C与D同主族短周期元素原子形成个数比为1:1的化合物,其电子 式 。
(4) BE3在常温下是一种淡黄色的液体,遇水即发生水解可生成一种具有漂白性的物质和一种有刺激性气味气体,写出该反应的方程式 ;
(5)下列事实能证明D与E非金属性强弱的是 (选填字母序号)。
A.常温下,D的单质呈固态,E的单质呈气态
B.E的氢化物的稳定性强于D的氢化物
C.E与D形成的化合物中,D呈正价
D.E的氢化物的沸点高于D的氢化物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下学期期中考试化学试卷(解析版) 题型:选择题
恒温恒容时,将NO2与SO2以体积比1:2置于密闭容器中发生反应:NO2(g)+SO2(g) SO3(g)+NO(g)下列能说明反应达到平衡状态的是( )
SO3(g)+NO(g)下列能说明反应达到平衡状态的是( )
A.体系压强保持不变
B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变
D.每消耗1 mol SO3的同时生成1 molNO2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下学期期中考试化学试卷(解析版) 题型:选择题
下列关于反应能量的说法正确的是( )
A.Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s) ΔH=-216 kJ·mol-1 ,则反应物总能量大于生成物总能量
B.若一定条件下,A=B ΔH<0,说明A物质比B物质稳定
C.101 kPa时,2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ·mol-1 ,则H2的燃烧热为571.6 kJ·mol-1
D.H+ (aq)+OH- (aq)=H2O(l) ΔH=-57.3 kJ·mol-1 ,含1 mol NaOH的溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ的热量.
查看答案和解析>>
科目:高中化学 来源:2016届云南省高三下第七次月考理综化学试卷(解析版) 题型:填空题
高纯六水氯化锶晶体(SrCl2•6H2O)具有很高的经济价值,工业上用w kg难溶于水的的碳酸锶(SrCO3)为原料(含少量钡和铁的化合物等),共制备高纯六水氯化锶晶体(a kg)的过程为:
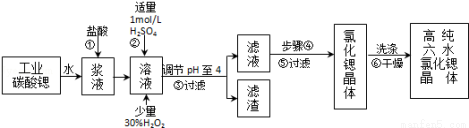
已知:Ⅰ.SrCl2•6H2O晶体在61℃时开始失去结晶水,100℃时失去全部结晶水.
Ⅱ.有关氢氧化物开始沉淀和完全沉淀的pH表:

(1)操作①加快反应速率的措施有________________ (写一种)。操作①中盐酸能否改用硫酸,其理由是:
(2)酸性条件下,加入30% H2O2溶液,将Fe2+氧化成Fe3+,其离子方程式为________.
(3)在步骤②﹣③的过程中,将溶液的pH值由1调节至4时,宜用的试剂为________.
A.氨水 B.氢氧化锶粉末 C. 氢氧化钠 D.碳酸钠晶体
(4)操作③中所得滤渣的主要成分是________ (填化学式).
(5)工业上完成操作③常用的设备有:
A分馏塔 B 离心机 C 热交换器 D 反应釜
(6)工业上用热风吹干六水氯化锶,适宜的温度是____________
A.40~50℃ B.50~60℃ C.60~70℃ D.80℃以上.
(7)已知工业流程中锶的利用率为90%根据以上数据计算工业碳酸锶的纯度:
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三考前热身(五模)化学试卷(解析版) 题型:选择题
下列有关物质的性质与其应用不相对应的是
A.Al具有良好延展性和抗腐蚀性,可制成铝箔包装物品
B.二氧化硅有良好的导电性,是制造光导纤维的主要材料
C.药皂中加入少量苯酚,可以起到杀菌消毒的作用
D.碳酸钠溶液显碱性,可用热的纯碱溶液除去金属器件表面的油污
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com