为了证明一水合氨(NH
3?H
2O)是弱电解质,甲、乙、丙三人分别选用下列物质进行实验:0.010mol/L氨水、0.1mol/L NH
4Cl溶液、NH
4Cl晶体、酚酞试液、pH试纸、蒸馏水.
(1)甲用pH试纸测出0.010mol/L氨水的pH为l0,则认定一水合氨是弱电解质,你认为这一方法是否正确?
正确
正确
(填“正确”或“不正确”),并说明理由:
如果氨水是强碱,0.010mol?L-1氨水C(H+)=10-12mol/L,pH为12,实际上溶液的pH=10<12,所以氨水是弱碱
如果氨水是强碱,0.010mol?L-1氨水C(H+)=10-12mol/L,pH为12,实际上溶液的pH=10<12,所以氨水是弱碱
.
(2)乙取出10mL 0.010mol/L氨水,用pH试纸测其pH=a,然后用蒸馏水稀释至1 000mL,再用pH试纸测其pH=b.若要确认NH
3?H
2O是弱电解质,则a、b应满足什么关系?
a>b>a-2
a>b>a-2
.
(3)丙取出10mL 0.010mol/L氨水,滴入2滴酚酞试液,显粉红色,再加入少量NH
4Cl晶体,溶液颜色变
浅
浅
(填“深”或“浅”).你认为这一方法能否证明NH
3?H
2O是弱电解质?
能
能
(填“能”或“否”),并说明原因:
向氨水中加入氯化铵后,如果氨水是弱电解质,则抑制氨水的电离,溶液中氢氧根离子浓度降低,溶液的碱性减弱,则溶液的颜色变浅,则说明氨水存在电离平衡;
向氨水中加入氯化铵后,如果氨水是弱电解质,则抑制氨水的电离,溶液中氢氧根离子浓度降低,溶液的碱性减弱,则溶液的颜色变浅,则说明氨水存在电离平衡;
.
(4)请你根据所提供的试剂,再提出一个合理又简便的方案证明NH
3?H
2O是弱电解质:
选择0.1mol/L NH4Cl溶液和pH试纸,PH测定氯化铵溶液呈酸性,是因为铵根离子水解显酸性,说明一水合氨是弱电解质;
选择0.1mol/L NH4Cl溶液和pH试纸,PH测定氯化铵溶液呈酸性,是因为铵根离子水解显酸性,说明一水合氨是弱电解质;
.

 阅读快车系列答案
阅读快车系列答案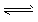 NH4++OH-,下列有关说法正确的是
NH4++OH-,下列有关说法正确的是