
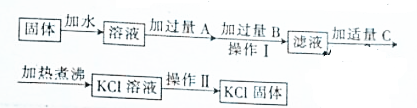
分析 利用MgCl2和MgSO4能与所提供的溶液中的Ba(OH)2溶液形成氢氧化镁沉淀、硫酸钡沉淀而被除去,因此可先向混合溶液中加入足量或过量的Ba(OH)2溶液,待充分反应后过滤,所得滤液为KCl溶液与过量Ba(OH)2溶液的混合溶液;接下来利用加入过量碳酸钾的方法再把多余的Ba(OH)2反应而除去,此时过滤后的溶液为KCl溶液、KOH溶液及过量的K2CO3溶液的混合溶液;然后利用KOH、K2CO3与HCl反应生成KCl采取滴加适量稀HCl到不再放出气泡时,得到的溶液即为纯净的KCl溶液,最后经蒸发结晶可得到氯化钾晶体,以此解答该题.
解答 解:(1)向混合溶液中加入过量的Ba(OH)2溶液,溶液中的MgCl2和MgSO4与Ba(OH)2发生反应而完全被除去;过滤后再向滤液中加入过量K2CO3溶液,与滤液中加入的过量的Ba(OH)2或反应生成的BaCl2反应而除去;过滤后再次向滤液中加入稀盐酸,稀盐酸与过量的K2CO3及反应生成的KOH反应生成KCl而得到纯净的KCl溶液;
故答案为:Ba(OH)2;K2CO3; HCl;
(2)①A为氢氧化钡,氢氧化钡可以将MgCl2、MgSO4中的镁离子和硫酸根离子除去,加入过量氢氧化钡,可使镁离子和硫酸根离子完全生成沉淀而除去,
故答案为:除去镁离子和硫酸根离子;
②加入过量的K2CO3溶液可使滤液中混有的Ba(OH)2或反应生成的BaCl2完全反应而除去,故答案为:除去过量的Ba(OH)2和生成的BaCl2;
③反应后加入盐酸除去KOH、K2CO3,加热煮沸,可除去HCl,故答案为:除去HCl;
(3)操作Ⅰ为过滤操作,用于分离沉淀和溶液,操作Ⅱ为物质的溶液获得晶体的方法,为蒸发结晶,
故答案为:过滤;蒸发结晶.
点评 本题考查物质的分离、提纯知识,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握实验的原理和操作方法,为解答该题的关键,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙烯的最简式C2H4 | B. | 四氯化碳的电子式  | ||
| C. | 乙烷的结构简式CH3CH3 | D. | 乙醛的结构简式CH3COH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 实验方法 | 实验现象 | 结论 |
| ① | 将氯水滴加到AgNO3溶液中 | a:有白色沉淀生成 | 氯水中含有Cl- |
| ② | 将氯水滴加到含有酚酞的NaOH溶液中 | 红色溶液变为无色 | |
| ③ | 将氯水滴加到Na2CO3溶液中 | b:有气泡产生 | 氯水中含有H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 反应前两种酸的物质的量浓度不同 | |
| B. | 反应开始后,盐酸的H+浓度减小快 | |
| C. | 反应开始后,醋酸的H+浓度减小快 | |
| D. | 从反应开始到结束,两种酸所用的时间相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{18}{{N}_{A}}$ | B. | $\frac{18g•mo{l}^{-1}}{{N}_{A}}$ | C. | 18NAg | D. | $\frac{18g}{{N}_{A}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30% | B. | 50% | C. | 70% | D. | 90% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L 0.1 mol•L-1的氨水含有0.1NA个OH- | |
| B. | 1 L 1 mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| C. | 25℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.1 NA | |
| D. | 在电解精炼粗铜的过程中,当阴极析出32 g铜时转移电子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com