
| X | ||||
| Y | Z | W |
| A. | X分别与Y、Z形成的化合物中化学键类型相同 | |
| B. | Z的最高价氧化物的水化物酸性比W的强 | |
| C. | X的简单气态氢化物的稳定性比W的弱 | |
| D. | 原子半径的大小顺序:r(Y)>r(Z)>r(W)>r(X) |
分析 由短周期主族元素X、Y、Z、W在元素周期表中的相对位置,可知X处于第二周期,Y、Z、W处于第三周期,X与Y最外层电子数相差4,设Y的最外层电子数为a,则X最外层电子数为a+4,则Y最高正化合价为+a,X的最低负化合价为(a+4)-8,X的最低负价与Y的最高正价代数和为零,故a+(a+4)-8=0,解得a=2,故Y为Mg,则Z为Si、W为P、X为O.
A.氧化镁为离子化合物,二氧化硅为共价化合物;
B.同周期自左而右非金属性增强,非金属性越强,最高价含氧酸的酸性越强;
C.同周期自左而右非金属性增强,同主族自上而下非金属性减弱,非金属性越强,氢化物越稳定;
D.同周期自左而右原子半径减小,同主族自上而下原子半径增大.
解答 解:由短周期主族元素X、Y、Z、W在元素周期表中的相对位置,可知X处于第二周期,Y、Z、W处于第三周期,X与Y最外层电子数相差4,设Y的最外层电子数为a,则X最外层电子数为a+4,则Y最高正化合价为+a,X的最低负化合价为(a+4)-8,X的最低负价与Y的最高正价代数和为零,故a+(a+4)-8=0,解得a=2,故Y为Mg,则Z为Si、W为P、X为O.
A.X分别与Y、Z形成的化合物为MgO、SiO2,MgO属于离子化合物,含有离子键,而SiO2属于共价化合物,含有共价键,故A错误;
B.非金属性W>Z,故Z的最高价氧化物的水化物酸性比W的弱,故B错误;
C.非金属性X>W,故X的简单气态氢化物的稳定性比W的强,故C错误;
D.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:r(Y)>r(Z)>r(W)>r(X),故D正确,
故选:D.
点评 本题考查结构性质位置关系应用,侧重对元素周期律的考查,熟练掌握元素周期表的结构,注意对基础知识的理解掌握.


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:选择题
| A. | 目前我国流通的硬币是由合金材料制造的 | |
| B. | 生铁、普通钢和不锈钢中的碳含量依次增加 | |
| C. | 装修门窗使用的铝合金材料的硬度比铝大,熔点比铝低 | |
| D. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
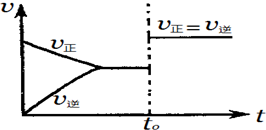
| A. | 若a+b=c,则t0时可能是增大反应体系的压强 | |
| B. | 若a+b=c,则t0时不可能是加入催化剂 | |
| C. | 若a+b≠c,则t0时只可能是加入催化剂 | |
| D. | 若a+b≠c,则t0时有可能是增大反应体系的压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | M点溶液中水的电离程度比原溶液小 | |
| B. | 在M点时,n(OH-)-n(H+)=(a-0.05)mol | |
| C. | 随着NaOH的加入,$\frac{c({H}^{+})}{c(N{H}_{4}^{+})}$不断增大 | |
| D. | 当n(NaOH)=0.1mol时,c(OH-)>c(Cl-)-c(NH3•H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 此白色固体不可能是KHCO3和KOH的混合物 | |
| B. | 此白色固体中含有K2CO36.90g | |
| C. | 原KOH溶液的物质的量浓度是0.500 mol•L-1 | |
| D. | 此白色固体可能为KOH和K2CO3的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去CO2中混有的少量CO,通入适量氧气后点燃 | |
| B. | 将混合气体通过灼热的铜网除去N2中的少量氧气 | |
| C. | 用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水 | |
| D. | 用盐酸除去AgCl中少量的Ag2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiH4分子呈正四面体形 | |
| B. | SiH4分子是非极性分子 | |
| C. | 因为Si-H键键能比C-H键键能低,所以SiH4沸点低于CH4沸点 | |
| D. | SiH4分子稳定性低于CH4分子,因为C-H键键能高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4LCl2完全溶于水时转移的电子数为NA | |
| B. | 1 mol 甲基(-CH3)含有的电子数为9NA | |
| C. | 100g30%醋酸溶液中氢原子数为2NA | |
| D. | 100mL水中OH-的个数是10-8NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com