印制线路板的生产原理是在一定规格的镀有铜膜的绝缘性基材上,根据需要在铜膜上画出线路并在线路上覆盖涂层保护线路,然后将其余全部浸入FeCl
3溶液将线路以外的铜腐蚀溶解而得.
(1)铜发生腐蚀的离子方程式为
;腐蚀废液中还含有Fe
3+,原因是
.
(2)为了从腐蚀印刷线路板的废液(含Fe
3+、Fe
2+、Cu
2+)中回收铜,并重新获得FeCl
3溶液,采用流程:
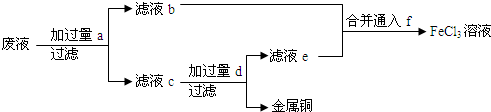
物质a为
(填化学式);通入f时反应的离子方程式是
.
(3)在一定量的废液中逐渐加入氨水至过量,最后所得溶液的颜色为
色;向溶液中加入一定量的乙醇有晶体析出,该晶体化学式是
(含1个结晶水).
(4)在滤液e中加入NaOH溶液会产生
色沉淀,将沉淀放置于空气中发生的反应的化学方程式为
.




 阅读快车系列答案
阅读快车系列答案