
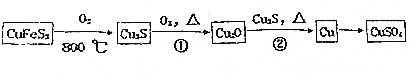
·ÖĪö £Ø1£©CuĪ»ÓŚµŚĖÄÖÜĘŚ¢õ¢ņB×壬ŹĒ29ŗÅŌŖĖŲ£¬»łĢ¬ĶŌ×ӵļŪµē×ÓÅŲ¼Ź½ĪŖ1s22s22p63s23p63d104s1£»Ķ¬Ö÷×åŌŖĖŲµŚŅ»µēĄėÄÜ×ŌÉĻ¶ųĻĀÖš½„¼õŠ”£»
£Ø2£©ÓÉ£Ø1£©·ÖĪöÖŖ·“Ó¦¢Ł¢ŚÉś³ÉµÄĻąĶ¬ĘųĢå·Ö×ÓŹĒSO2£¬SO2ÖŠ¼Ū²ćµē×Ó¶ŌøöŹż=2+$\frac{1}{2}$£Ø6-2”Į2£©=3£¬ĒŅŗ¬ÓŠŅ»øö¹Āµē×Ó¶Ō£¬ĖłŅŌĘäæռ乹ŠĶŹĒVŠĶ£¬SŌ×Ó²ÉÓĆsp2Ōӻƣ»
£Ø3£©ĮņĖįĶČÜŅŗÓė°±Ė®Éś³ÉĒāŃõ»ÆĶ£¬ĒāŃõ»ÆĶČÜÓŚ¹żĮæµÄ°±Ė®£¬ŠĪ³É[Cu£ØNH3£©4]2+Ąė×Ó£¬Ąė×ÓÖŠ“ęŌŚ¹²¼Ū¼ü”¢ÅäĪ»¼ü£®
½ā“š ½ā£ŗ£Ø1£©CuĪ»ÓŚµŚĖÄÖÜĘŚ¢õ¢ņB×壬ŹĒ29ŗÅŌŖĖŲ£¬»łĢ¬ĶŌ×ӵļŪµē×ÓÅŲ¼Ź½ĪŖ3d104s1£»Ķ¬Ö÷×åŌŖĖŲµŚŅ»µēĄėÄÜ×ŌÉĻ¶ųĻĀÖš½„¼õŠ”£¬ĖłŅŌµŚŅ»µēĄėÄܽĻ“óµÄŹĒŃõ£¬
¹Ź“š°øĪŖ£ŗ3d104s1£»O£»
£Ø2£©ÓÉ£Ø1£©·ÖĪöÖŖ·“Ó¦¢Ł¢ŚÉś³ÉµÄĻąĶ¬ĘųĢå·Ö×ÓŹĒSO2£¬SO2ÖŠ¼Ū²ćµē×Ó¶ŌøöŹż=2+$\frac{1}{2}$£Ø6-2”Į2£©=3£¬ĖłŅŌSŌ×Ó²ÉÓĆsp2Ōӻƣ¬ÓÉÓŚŗ¬ÓŠŅ»øö¹Āµē×Ó¶Ō£¬Ęäæռ乹ŠĶŹĒVŠĶ£¬
¹Ź“š°øĪŖ£ŗsp2£»VŠĶ£»
£Ø3£©ĮņĖįĶČÜŅŗÓė°±Ė®Éś³ÉĒāŃõ»ÆĶĄ¶É«³Įµķ£¬ĒāŃõ»ÆĶČÜÓŚ¹żĮæµÄ°±Ė®£¬ŠĪ³É[Cu£ØNH3£©4]2+Ąė×Ó£¬Ą¶É«³ĮµķČÜÓŚ°±Ė®µÄĄė×Ó·½³ĢŹ½ĪŖCu£ØOH£©2+4NH3•H2O=[Cu£ØNH3£©4]2++2OH-+4H2O£¬ÉīĄ¶É«ĶøĆ÷ČÜŅŗÖŠµÄŃōĄė×ӣز»æ¼ĀĒH+£©ÄŚ“ęŌŚµÄČ«²æ»Æѧ¼üĄąŠĶÓŠ¹²¼Ū¼ü”¢ÅäĪ»¼ü£¬
¹Ź“š°øĪŖ£ŗCu£ØOH£©2+4NH3•H2O=[Cu£ØNH3£©4]2++2OH-+4H2O£»¹²¼Ū¼ü”¢ÅäĪ»¼ü£®
µćĘĄ ±¾Ģāæ¼²éĮĖÅäĪ»»ÆŗĻĪļ³É¼üĒéæö£¬ĢāÄæÄѶČÖŠµČ£¬Éę¼°ŗĖĶāµē×ÓÅŲ¼”¢µēøŗŠŌ”¢ÅäĪ»»ÆŗĻĪļµČÖŖŹ¶£¬Ć÷Č·ÅäĪ»»ÆŗĻĪļµÄ³É¼üĒéæöĪŖ½ā“š¹Ų¼ü£¬ŹŌĢāÅąŃųĮĖѧɜµÄĮé»īÓ¦ÓĆÄÜĮ¦£®


 »ĘøŌŠ”דŌŖ½ā¾öĪŹĢāĢģĢģĮ·ĻµĮŠ“š°ø
»ĘøŌŠ”דŌŖ½ā¾öĪŹĢāĢģĢģĮ·ĻµĮŠ“š°ø ČżµćŅ»²āæģĄÖÖÜ¼Ę»®ĻµĮŠ“š°ø
ČżµćŅ»²āæģĄÖÖÜ¼Ę»®ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ūĶéČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗC3H8£Øg£©+5O2£Øg£©=3CO2£Øg£©+4H2O£Øg£©£»”÷H=-2221.5 kJ•mol-1 | |
| B£® | Õż¶”ĶéČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗ2C4H10£Øg£©+18O2£Øg£©=8CO2£Øg£©+10H2O£Øl£©£»”÷H=-2878 kJ•mol-1 | |
| C£® | Õż¶”Ķé×Ŗ»ÆĪŖŅģ¶”ĶéµÄ¹ż³ĢŹĒŅ»øö·ÅČČ¹ż³Ģ | |
| D£® | Õż¶”Ķé±ČŅģ¶”ĶéĪČ¶Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
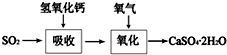 ¹¤ŅµÉĻ³£²śÉś“óĮæµÄ·ĻĘų”¢·ĻĖ®”¢·ĻŌü”¢·ĻČČ£¬Čē¹ū“¦Ąķ²»ŗĆ£¬ĖęŅāÅÅ·Å£¬»įŌģ³ÉĪŪČ¾£¬¶ųČē¹ūæĘѧ»ŲŹÕ£¬æɱä·ĻĪŖ±¦£®
¹¤ŅµÉĻ³£²śÉś“óĮæµÄ·ĻĘų”¢·ĻĖ®”¢·ĻŌü”¢·ĻČČ£¬Čē¹ū“¦Ąķ²»ŗĆ£¬ĖęŅāÅÅ·Å£¬»įŌģ³ÉĪŪČ¾£¬¶ųČē¹ūæĘѧ»ŲŹÕ£¬æɱä·ĻĪŖ±¦£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ¢ńŗĶ¢ņ | B£® | ¢ņŗĶ¢ó | C£® | ¢óŗĶ¢ō | D£® | ¢ńŗĶ¢ō |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
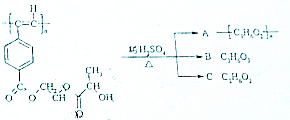 ¾ŪŅŅČ²µ¼µē¾ŪŗĻĪļµÄŗĻ³ÉŹ¹øß·Ö×Ó²ÄĮĻ½ųČėĮĖ”°ŗĻ³É½šŹō”±ŗĶĖÜĮĻµē×ÓѧŹ±“ś£¬ČēĶ¼ŹĒ¾ŪŅŅČ²ŃÜÉśĪļ·Ö×ÓMµÄ½į¹¹Ź½¼°MŌŚĻ”ĮņĖį×÷ÓĆĻĀµÄĖ®½āŹ¾ŅāĶ¼£ŗ
¾ŪŅŅČ²µ¼µē¾ŪŗĻĪļµÄŗĻ³ÉŹ¹øß·Ö×Ó²ÄĮĻ½ųČėĮĖ”°ŗĻ³É½šŹō”±ŗĶĖÜĮĻµē×ÓѧŹ±“ś£¬ČēĶ¼ŹĒ¾ŪŅŅČ²ŃÜÉśĪļ·Ö×ÓMµÄ½į¹¹Ź½¼°MŌŚĻ”ĮņĖį×÷ÓĆĻĀµÄĖ®½āŹ¾ŅāĶ¼£ŗ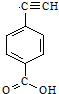 £»
£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.30 | B£® | 0.35 | C£® | 0.40 | D£® | 0.50 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com