
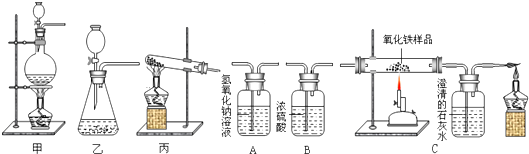
分析 (1)装置乙为固液不需加热制备气体的装置,实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳;检查装置乙气密性的方法是:关闭分液漏斗的活塞后,先把导管的一端插入水中,然后两手紧握锥形瓶的外壁,观察导管口有气泡冒出,松开手后,导管口会倒吸上升一段水柱,则说明装置乙气密性好;
(2)①草酸(H2C2O4)与浓硫酸混合加热会产生一氧化碳,因此需要加热,则应选择液液加热型装置;
②草酸(H2C2O4)与浓硫酸混合加热生成一氧化碳和二氧化碳和水,因此草酸加热后的气体生成物是一氧化碳和二氧化碳,要得到干燥、纯净的一氧化碳,应该先除杂质二氧化碳,然后再干燥,据此分析;
③能证明CO气体具有还原性的实验现象是:C中红色变黑色,澄清石灰水变浑浊;
④不能说明5.6克一氧化碳是否都与氧化铁反应,因此无法应用5.6克一氧化碳计算;根据反应前后澄清石灰水增重6.6克,即二氧化碳的质量是6.6g,然后根据二氧化碳的质量求氧化铁的质量,最后求氧化铁的质量分数.
解答 解:(1)实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,不需要加热的固液反应,可用装置乙来制备;
检查装置乙气密性的方法是:关闭分液漏斗的活塞后,先把导管的一端插入水中,然后两手紧握锥形瓶的外壁,观察导管口有气泡冒出,松开手后,导管口会倒吸上升一段水柱,则说明装置乙气密性好;
故答案为:CaCO3+2HCl=CaCl2+CO2↑+H2O;关闭分液漏斗的活塞后,先把导管的一端插入水中,然后两手紧握锥形瓶的外壁,观察导管口有气泡冒出,松开手后,导管口会倒吸上升一段水柱,则说明装置乙气密性好;
(2)①草酸(H2C2O4)与浓硫酸混合加热会产生一氧化碳,因此需要加热;则应选择液液加热型装置甲,故答案为:甲;
②草酸(H2C2O4)与浓硫酸混合加热生成一氧化碳和二氧化碳和水,因此草酸加热后的气体生成物是一氧化碳和二氧化碳;要得到干燥、纯净的一氧化碳,应该先除杂质二氧化碳,然后再干燥,所以应先通A氢氧化钠吸收二氧化碳再通B浓硫酸干燥,后通C装置还原,故答案为:A、B、C;一氧化碳、二氧化碳;
③能证明CO气体具有还原性的实验现象是:C中红色变黑色,澄清石灰水变浑浊;故答案为:C中红色变黑色,澄清石灰水变浑浊;
④数据一测量中,不能说明5.6克一氧化碳是否都与氧化铁反应,因此无法应用5.6克一氧化碳计算;
因此应该用反应前后澄清石灰水增重6.6克,即二氧化碳的质量是6.6g,设氧化铁的质量分数为x
3CO+Fe2O3 2Fe+3CO2
160 3×44
12x 6.6g x≈66.7%
故答案为:66.7%.
点评 本考点主要考查了检查装置的气密性、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和有关的计算等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关,气体的收集装置的选择与气体的密度和溶解性有关.


科目:高中化学 来源: 题型:选择题
| A. | v(CO)=0.025 mol•L-1•S-1 | B. | v(NO2)=0.7 mol•L-1•min-1 | ||
| C. | v(N2)=0.36 mol•L-1•min-1 | D. | v(CO2)=1.1 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当反应相同体积的CH4时反应①②转移的电子数相同 | |
| B. | 由反应①可推知:CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(l)△H>-574 kJ•mol-1 | |
| C. | 反应②中当生成4.48 L CO2时转移的电子总数为1.60 mol | |
| D. | 若用标准状况下4.48 L CH4还原NO2生成N2和水蒸气,放出的热量为173.4 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间内生成n mol H2,同时生成n mol I2 | |
| B. | 容器内压强不随时间而变化 | |
| C. | 单位时间内生成2n mol HI,同时生成n mol I2 | |
| D. | 混合气体的平均分子量不随时间而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第三周期元素的离子半径从左到右逐渐减小 | |
| B. | 第二周期元素从左到右,最高正价从+1递增到+7 | |
| C. | 同主族元素的简单阴离子还原性越强,对应单质的氧化性越强 | |
| D. | ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽马鞍山二中高一10月阶段测化学卷(解析版) 题型:选择题
同温同压下,相同体积的甲、乙两种气体的质量比为17:14,若乙气体是CO,则甲气体可能为
A.H2S B.HCl C.NH3 D.Cl2
查看答案和解析>>
科目:高中化学 来源:2017届云南省高三上第二次周考化学试卷(解析版) 题型:选择题
下列实验方案设计正确的是
A.分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤
B.失去标签的硝酸银溶液、稀盐酸、氢氧化钠溶液、氧化铝溶液,可以用碳酸钱溶液鉴别
C.将CuC12溶液在蒸发皿中加热蒸千,得到无水CuCl2固体
D.检验从火星上带回来的红色物体是否是Fe2O3的操作步骤为:样品 粉碎
粉碎 加水溶解
加水溶解 过滤
过滤 向滤液中滴加KSCN 溶液
向滤液中滴加KSCN 溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com