


科目:高中化学 来源: 题型:
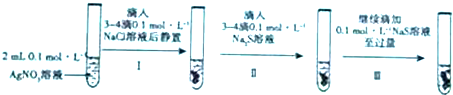
| A、2mol/L |
| B、0.2 mol/L |
| C、0.02 mol/L |
| D、20 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用新制Cu(OH)2检验尿糖 |
| B、用糯米、酒曲和水制甜酒 |
| C、用食醋除去水壶中的水垢 |
| D、苯使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)高中教材中有这样一个实验:如图,在两支试管中分别加入3mL稀盐酸,将两个各装有0.3g NaHCO3或Na2CO3粉末的小气球分别套在两支试管口.将气球内的NaHCO3或Na2CO3粉末同时倒入试管中,观察到现象如下:
(1)高中教材中有这样一个实验:如图,在两支试管中分别加入3mL稀盐酸,将两个各装有0.3g NaHCO3或Na2CO3粉末的小气球分别套在两支试管口.将气球内的NaHCO3或Na2CO3粉末同时倒入试管中,观察到现象如下:| 序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后最高或最低温度 |
| ① | 35mL水 | 2.5gNaHCO3固体 | 20℃ | 18.5℃ |
| ② | 35mL水 | 2.5g Na2CO3固体 | 20℃ | 24.3℃ |
| ③ | 35mL稀盐酸 | 含2.5g NaHCO3的饱和溶液32.5mL | 20℃ | 19℃ |
| ④ | 35mL稀盐酸 | 含3.2g Na2CO3的饱和溶液23.1mL+10mL水 | 20℃ | 24.2℃ |
| ⑤ | 35mL稀盐酸 | 2.5g NaHCO3固体 | 20℃ | 16.2℃ |
| ⑥ | 35mL稀盐酸 | 2.5g Na2CO3固体 | 20℃ | 25.1℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
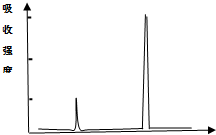 某有机物可作为无铅汽油的抗爆剂,质谱法测得其最大质荷比为88.0,取该有机物8.8g完全燃烧,将产物通过依次通过浓硫酸和碱石灰,测得增重分别为10.8g和22g,
某有机物可作为无铅汽油的抗爆剂,质谱法测得其最大质荷比为88.0,取该有机物8.8g完全燃烧,将产物通过依次通过浓硫酸和碱石灰,测得增重分别为10.8g和22g,查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2 |
| B、CH4 |
| C、CO |
| D、HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com