
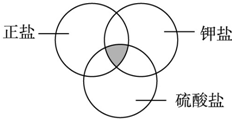
| A、KNO3 |
| B、KHSO4 |
| C、K2S |
| D、K2SO4 |


科目:高中化学 来源: 题型:
| A、54g | B、57.8g |
| C、47.8g | D、33.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.34mol |
| B、0.38mol |
| C、0.28mol |
| D、0.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol 氧气中含有12.04×1023个氧原子,在标准状况下占有体积22.4 L |
| B、1 mol臭氧和1.5 mol氧气含有相同的氧原子数 |
| C、等体积、浓度均为1 mol/L的硫酸和盐酸,电离出的氢离子数之比为2:1 |
| D、氧原子数之比为1:6的干冰和葡萄糖(C6H12O6),其碳原子数之比也为1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,33.6L HF中含有氟原子的数目为1.5NA |
| B、常温常压下,9.2g二氧化氮和四氧化二氮的混合物含有氮原子的数目为0.2NA |
| C、50mL18.4mol?L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
| D、0.1mol铁溶于足量氯水中,转移电子的总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在化学变化中,原子的核电荷数和核外电子数都不发生改变 |
| B、未见饭菜就闻到饭菜的香味,说明物质的分子很小,且在不停地运动 |
C、某粒子示意图 ,表示的是一种金属阳离子 ,表示的是一种金属阳离子 |
| D、构成金刚石、石墨、C60等碳单质的原子,其核内质子数都为6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com