
【题目】在制取水泥、玻璃的生产中,共同使用的主要原料是
A. Na2CO3 B. 石灰石 C. 石英 D. 焦炭
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】下列关于过滤的叙述正确的是( )
A. 过滤所需实验用品有漏斗、烧杯、玻璃棒、铁架台(带铁圈)
B. 过滤时把漏斗放在铁三脚架上
C. 过滤时将玻璃棒斜靠在三层滤纸上
D. 过滤时为了加快过滤速度,用玻璃棒搅拌过滤器中的液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于实验Ⅰ~Ⅳ的描述不正确的是
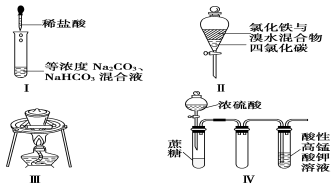
①实验Ⅰ:逐滴滴加稀盐酸时,试管中开始没有立即产生大量气泡
②实验Ⅱ:充分振荡后静置,下层溶液为橙红色,上层无色
③实验Ⅲ:从饱和食盐水中提取氯化钠晶体
④实验Ⅳ:酸性KMnO4溶液中有气泡出现,且溶液颜色逐渐变浅乃至褪去
A.②③ B.①② C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3的催化氧化是工业制取硝酸的关键步骤之一,该反应的化学方程式为:
4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),△H<0。
4NO(g)+6H2O(g),△H<0。
请回答下列问题:
(1)在恒温恒容下判断该反应达到平衡状态的标志是________(填字母)。
a.NH3和NO浓度相等
b.NO百分含量保持不变
c.容器中气体的压强不变
d.NH3的生成速率与NO的消耗速率相等
(2)当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高NH3平衡转化率的是_____________。(填字母)
a.向装置中再充入N2 b.向装置中再充入O2 c.改变反应的催化剂 d.降低温度
(3)将0.050 mol NH3 (g)和0.060 mol O2(g)放入容积为1L的密闭容器中,在一定条件下达到平衡,测得c(NO)=0.040 mol/L。计算该条件下反应的NH3的转化率和写出平衡常数K 的表达式(不必写出计算过程)。
①平衡常数的表达式K=________________;
②平衡时,NH3的转化率α(NH3 )=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应mA(g)+nB![]() pC(g)+qD中,A和C都是无色气体,达到平衡后,下列叙述正确的是
pC(g)+qD中,A和C都是无色气体,达到平衡后,下列叙述正确的是
A.若增加B的量,平衡体系颜色加深,说明B必是气体
B.增大压强,平衡不移动,说明m+n一定等于p+q
C.升高温度,A的转化率减小,说明正反应是吸热反应
D.若B是气体,增大A的量,A、B的转化率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有体积相同、相等pH的烧碱溶液和氨水,下列叙述中正确的是
A. 两溶液物质的量浓度相同
B. 两溶液中OH-离子浓度相同
C. 用同浓度的盐酸中和时,消耗盐酸的体积相同
D. 加入等体积的水稀释后,pH仍相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)水(H2O)在很多化学反应中具有极其重要的作用。请研究下列水参与的氧化还原反应。 ①NaH+H2O=NaOH+H2↑
②2Na2O2+2H2O=4NaOH+O2↑
③2Na+2H2O =2NaOH+H2↑
④3NO2+H2O=2HNO3+NO
⑤2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
⑥2F2+2H2O=4HF+O2
水只作氧化剂的是____________;水只作还原剂的是____________;水既作氧化剂,又作还原剂的是____________;水既不作氧化剂,又不是还原剂的是____________。
(2)KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为:2KClO3+4HCl (浓)=2KCl+2ClO2↑+Cl2↑+2H2O。
①请分析该反应中电子转移的情况(用双线桥法表示)。
②浓盐酸在反应中显示出来的性质是________(填序号)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③若产生0.1 mol Cl2,则转移的电子的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物命名正确的是( )
A. 1,3-二甲基丁烷 B. 2,3,5-三甲基己烷
C. 2,3-二甲基-2-乙基己烷 D. 2,3-二甲基-4-乙基戊烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com