
| ||
| △ |
| 112mol |
| 4 |
| ||
| △ |
| 5 |
| 4 |
| 4 |
| 3 |


科目:高中化学 来源: 题型:
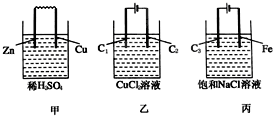 甲、乙、丙三个烧杯中分别装有稀硫酸、氯化铜溶液、饱和食盐水,把用导线连接的锌片和铜片插入甲,把分别与直流电流正、负极相连的C1、C2插入乙,把分别与直流电源正、负极相连的C3、铁片插入丙.(C1、C2、C3为石墨棒)则下列叙述正确的是( )
甲、乙、丙三个烧杯中分别装有稀硫酸、氯化铜溶液、饱和食盐水,把用导线连接的锌片和铜片插入甲,把分别与直流电流正、负极相连的C1、C2插入乙,把分别与直流电源正、负极相连的C3、铁片插入丙.(C1、C2、C3为石墨棒)则下列叙述正确的是( )| A、甲、丙中是化学能转变为电能,乙中是电能转变为化学能 |
| B、C1、C2分别是阳极、阴极,锌片、铁片上都发生氧化反应 |
| C、C1和C3放出的气体相同,铜片和铁片放出的气体也相同 |
| D、甲、丙中溶液的pH值都逐渐升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
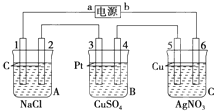 如图,通电5min后,电极5质量增加2.16g,回答:
如图,通电5min后,电极5质量增加2.16g,回答:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、非金属单质在反应中只作氧化剂 |
| B、肯定有一种元素被氧化,另一种元素被还原 |
| C、在反应中不一定所有元素的化合价都发生变化 |
| D、金属原子失电子越多,其还原性越强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com