
【题目】下列关于乙醇的说法中,不正确的是
A.乙醇是无色透明、有特殊香味的液体 B.乙醇可以使酸性高锰酸钾溶液褪色
C.乙醇属于烃类物质 D.无水硫酸铜常用于检验乙醇中是否含有水
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g)+2CO(g) ![]() 2CO2(g)+S(l) ΔH<0,
2CO2(g)+S(l) ΔH<0,
若反应在恒容的密闭容器中进行,下列有关说法正确的是
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应的平衡常数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
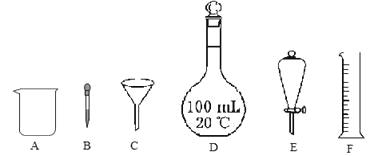
(1)下列各组混合物中,能用仪器E进行分离的是 (填序号)。
a.水和四氯化碳 b.水和酒精 c.水中的泥沙
(2)配制100mL 0.1 mol·L-1NaOH溶液,所需氢氧化钠固体的质量是 g。实验中用到的上述仪器有 (填序号),还缺少的玻璃仪器是 (填仪器名称)。
Ⅱ、现有下列四种物质,①H2 ②Cl2 ③SO2 ④H2SO4
请回答相关问题:

(1)如右图所示,从B口进气可收集的气体是 (填序号,下同)。
(2)能使品红溶液褪色且加热时又复原的是 ;属于电解质的是 ;能与水发生氧化还原反应的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下(已知2KI+Cl2===2KCl+I2,碘与溴一样易溶于有机溶剂):
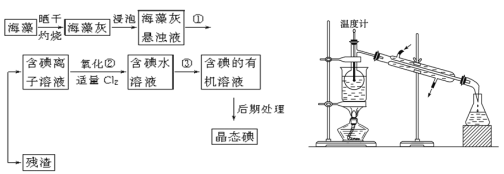
(1)指出提取碘的过程中有关的实验操作名称:①____________,③_____________。
(2)提取碘的过程中,可供选择的有机试剂是____________。
A.苯 B.四氯化碳 C.酒精
(3)为使上述流程中含碘离子溶液转化为碘的有机溶液,实验室里有烧杯、玻璃棒以及必要的夹持仪器,尚缺少的玻璃仪器是 。
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出上图所示实验装置中的错误之处:
① 。
② 。
③ 。
(5)进行上述蒸馏操作时使用水浴的原因是 。
(6)四氯化碳是_________色液体。如果本实验用苯做萃取剂,则上层液体的颜色为 色,下层液体中溶质的主要成分为____________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组欲利用CuO与NH3的反应研究NH3的性质与分子组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
(1)仪器a的名称为 ;仪器b中的试剂不能为下列中的 (填字母)
A.氧化钙 B.碱石灰 C.石灰石 D.生石灰

(2)装置B的作用是
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管收集到无色无味的气体,上述现象证明了NH3具有 性,写出装置C中发生反应的化学方程式
(4)E装置中浓硫酸的作用 (写出一条即可)
(5)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比为 (用含m、n字母的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜.请根据下列流程图,完成回收硫酸亚铁和铜的实验方案.(可供选择的试剂为铁粉、稀H2SO4、NaOH溶液等试剂)

(1)操作a的名称为 ,所需要的玻璃仪器为 。
(2)固体E的成分为 ,加入的试剂④为稀硫酸,发生的化学方程式为 。
(3)加入试剂①的目的是 。
(4)从溶液D和溶液G中得到FeSO47H2O晶体的操作为 、冷却结晶、过滤、 、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铈、铬、钛、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。
(1)二氧化铈 (CeO2)在平板电视显示屏中有着重要应用。CeO2在稀硫酸和H2O2的作用下可生成Ce3+,CeO2在该反应中作__________剂。
(2)自然界Cr主要以+3价和+6价存在。+6价的Cr能引起细胞的突变,可以用亚硫酸钠将其还原为+3价的铬。完成并配平下列离子方程式:
_____Cr2O72-+_____SO32-+_____ =_____Cr3++_____SO42-+ _____H2O
(3)钛(Ti)被誉为“二十一世纪的金属”,工业上在550℃时用钠与四氯化钛反应可制得钛,该反应的化学方程式是 。
(4)NiSO4·xH2O是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀渣(除镍外,还含有铜、锌、铁等元素)为原料获得。操作步骤如下:
①向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质,除去Cu2+的离子方程式为_____________________。
②对滤液Ⅱ先加H2O2再调pH,调pH的目的是 _。
③滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com