
����Ŀ���������Ϊ10mL�����ʵ���Ũ����ͬ������NaOH��Һ�зֱ�ͨ��һ������CO2�õ���Һ���ҡ���ס�������Һ�зֱ�μ�0��1 mol��L-1���ᣬ��ʱ��Ӧ����CO2�������״�������������������Ĺ�ϵ��ͼ��ʾ����������������ȷ����

A. ԭNaOH��Һ�����ʵ���Ũ��Ϊ0.5 mol��L-1
B. ��0<V(HCl)<10mLʱ������Һ�з�����Ӧ�����ӷ���ʽΪOH-+H+=H2O
C. ����Һ�к��е�������Na2CO3��NaHCO3
D. ����Һ�еμ���������CO2��������ֵΪ224mL����״����
���𰸡�A
��������
������������Һ��ͨ��һ�����Ķ�����̼����Һ�����ʵ���ɿ�����NaOH��Na2CO3��Na2CO3��Na2CO3��NaHCO3��NaHCO3���������û�в���������̼ʱ�ķ�Ӧ����Ϊ��OH-+H+=H2O��CO32-+H+=HCO3-������������̼�ķ�ӦΪ��HCO3-+H+=H2O+CO2����A������ͼ���֪����V(HCl)=50mLʱ���õ��IJ���ΪNaCl����ԭ���غ��֪��n(NaOH)=n(NaCl)=n(HCl)=0.1mol/L��0.05L=0.005mol����ԭ����������Һ��Ũ��Ϊ��c(NaOH)=![]() =0.5mol/L����A��ȷ��B��������������Һ��ͨ��һ�����Ķ�����̼����Һ�����ʵ���ɿ����ǣ�NaOH��Na2CO3��Na2CO3��Na2CO3��NaHCO3��NaHCO3�����������ͼ��HCl �����������������̼��������Ĺ�ϵ��֪����Һ������Ӧ��Ϊ��Na2CO3��NaHCO3�����Ե�0��V(HCl)��10mLʱ������Һ��û�в���������̼�����ӷ���ʽΪ��CO32-+H+=HCO3-����B����C������������Һ��ͨ�������̼�����ʲ�����ΪNaOH��NaHCO3������ͼ���֪������Һ�е�����ΪNaOH��Na2CO3����C����D������Һ�еμ����ᣬ����������̼�Ľ�Ϊ��HCO3-+H+=H2O+CO2��������������10mL�����֪�����ɶ�����̼�����ʵ���Ϊ��0.1mol/L��0.01L=0.001mol�������0.001mol������̼�����ʵ���Ϊ��22.4L/mol��0.001mol=22.4mL����D����ѡA��
=0.5mol/L����A��ȷ��B��������������Һ��ͨ��һ�����Ķ�����̼����Һ�����ʵ���ɿ����ǣ�NaOH��Na2CO3��Na2CO3��Na2CO3��NaHCO3��NaHCO3�����������ͼ��HCl �����������������̼��������Ĺ�ϵ��֪����Һ������Ӧ��Ϊ��Na2CO3��NaHCO3�����Ե�0��V(HCl)��10mLʱ������Һ��û�в���������̼�����ӷ���ʽΪ��CO32-+H+=HCO3-����B����C������������Һ��ͨ�������̼�����ʲ�����ΪNaOH��NaHCO3������ͼ���֪������Һ�е�����ΪNaOH��Na2CO3����C����D������Һ�еμ����ᣬ����������̼�Ľ�Ϊ��HCO3-+H+=H2O+CO2��������������10mL�����֪�����ɶ�����̼�����ʵ���Ϊ��0.1mol/L��0.01L=0.001mol�������0.001mol������̼�����ʵ���Ϊ��22.4L/mol��0.001mol=22.4mL����D����ѡA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС������ͼ��ʾװ�òⶨ��þ�Ͻ������������������������ԭ��������
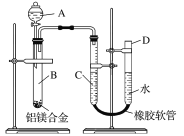
��1��A���Լ�Ϊ________��
��2��ʵ��ǰ���Ƚ���þ�Ͻ���ϡ���н���Ƭ�̣���Ŀ����________________________________��
��3����ҩƷ��ˮװ��������У����Ӻ�װ�ú�����еIJ������Тټ�¼C��Һ��λ�ã��ڽ�B��ʣ�������ˡ�ϴ�ӡ�������أ��۴�B�в���������������ָ������º�¼C��Һ��λ�ã�����A��B�еμ������Լ����ݼ�������ԡ�����������˳����____________(�����)����¼C��Һ��λ��ʱ��������ƽ���⣬��Ӧ___________________________��
��4��B�з�����Ӧ�Ļ�ѧ����ʽΪ____________________________________________________��
��5����ʵ���õ���þ�Ͻ������Ϊa g������������Ϊb mL(�ѻ���Ϊ��״��)��B��ʣ����������Ϊc g�����������ԭ������Ϊ________��
��6��ʵ������У���δϴ�ӹ������õIJ����������������������______(�ƫ��ƫС������Ӱ�족)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ɢϵ��������ɢϵ�ı��ʲ���ǣ�������
A.��ɢ��ֱ����С
B.�Ƿ��ж��������
C.�Ƿ��ȶ�
D.��ɢ�������Ƿ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʢ�е�ˮ���Թ��У���������CCl4��������Ƭ�̺�����
A.������Һ����ɫ
B.����Һ��Ϊ�ػ�ɫ
C.�ϲ�Ϊ��ɫ�²�Ϊ�Ϻ�ɫ
D.�²���ɫ�ϲ��Ϻ�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����2HI+Cl2=2HCl+I2����2Fe+3Cl2=2FeCl3����2FeBr2+3Cl2=2FeCl3+2Br2����һ��������HI��Fe��FeBr2�ֱ���������Cl2��Ӧ�����������Ӧ����ת����Ŀ��ȣ���HI��Fe��FeBr2�����ʵ���֮��Ϊ
A. 1��1��1 B. 1��3��3 C. 3��1��1 D. 6��3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�飬����˵��������������ʵ���
A. ����ʱ�������������Һ��pH��7
B. ����ʱ�����0.1 mol��L-1������Һ��pHԼΪ3
C. ������Һ�����ʯ��Ӧ��������
D. ��ͬ�¶��£����ͬ���ʵ���Ũ�ȵ�������Һ�ĵ����Ա�������Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʯī�ͽ��ʯ����̼Ԫ�صĵ��ʣ���֪C(ʯī��s)��C(���ʯ��s) ��H>0,����˵����ȷ����
A. ʯī������ʯ�ȶ�
B. ��������ʯī����ʯ��ȫȼ�գ����߷ų����������
C. ��������ʯī����ʯ��ȫȼ�գ����ʯ�ų���������
D. ���ʯ����ʯī�ȶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ������
A. ��ҵ��ұ�������뽹̿��Ŀ��������̿�����������������л�ԭ����
B. ��ҵ�Ʋ��������������ж�Ҫ����ʯ��ʯ��Ŀ���dz�ȥ���ʶ�������
C. ��ҵ���ý�������TiCl4��Һ�ڸ����·�Ӧ��Ŀ���ǽ������Ѵ��Ȼ������û�����
D. ��ˮ����ȡþ�Ĺ����м��뱴�������Ƶõ�ʯ�ң�Ŀ���ǽ�Mg2��ת���Mg(OH)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��M��W��Q��R��7�ֶ�����Ԫ�أ���ԭ�Ӱ뾶����Ҫ���ϼ����£�
Ԫ�ش��� | X | Y | Z | M | W | Q | R |
ԭ�Ӱ뾶/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
��Ҫ���ϼ� | +1 | +3 | +6����2 | +7����1 | +5����3 | ��2 | +1 |
���������գ�
��1������Ԫ���У���������ǿ�������ڱ��е�λ����________________________________��X��Y��Q�����γɵļ������������Ӱ뾶�ɴ�С��˳����_______(�����ӷ���)��
W��R��ԭ�Ӹ�����1�s4���ɵ������������Ļ�ѧ����____________________��
��2����������4�ֵ�������Ԫ�ص�����������ˮ���������������_______(�ѧ
ʽ)������뷽��ʽΪ_____________________________________��
��3��M��Z��ȣ��ǽ����Խ�ǿ����_____________����Ԫ�����ƣ������ԭ�ӽṹ�ĽǶ�˵������_________________________________________________________________��
��4����ϡ�����У�KMnO4��H2O2�ܷ���������ԭ��Ӧ����Ӧ����ʽ���£�
![]() KMnO4��
KMnO4��![]() H2O2+
H2O2+![]() H2SO4 ��
H2SO4 �� ![]() K2SO4��
K2SO4��![]() MnSO4��
MnSO4��![]() O2����
O2����![]() H2O
H2O
����ƽ������0.5 mol H2O2�μӴ˷�Ӧ������ת�Ƶĸ���Ϊ______________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com