
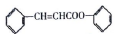 是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如图所示:
是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如图所示: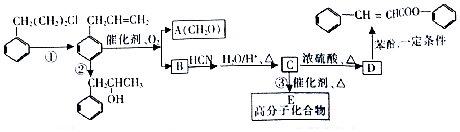
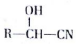 $→_{△}^{H_{2}O/H+}$
$→_{△}^{H_{2}O/H+}$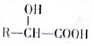
 $→_{△}^{催化剂}$
$→_{△}^{催化剂}$ +nH2O.
+nH2O. (任写一种).
(任写一种).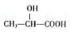 )的路线(其他试剂任选,合成路线常用的表示方式为A$\stackrel{反应试剂}{→}$B…$\stackrel{反应试剂}{→}$目标产物)
)的路线(其他试剂任选,合成路线常用的表示方式为A$\stackrel{反应试剂}{→}$B…$\stackrel{反应试剂}{→}$目标产物) 分析 根据流程图知,①为消去反应、②为加成反应、③发生信息i的氧化反应,则A为HCHO、B为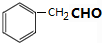 ,B发生信息ii的反应,C结构简式为
,B发生信息ii的反应,C结构简式为 ,C发生缩聚反应生成E,E结构简式为
,C发生缩聚反应生成E,E结构简式为 ,C发生消去反应生成D,D结构简式为
,C发生消去反应生成D,D结构简式为 ,D和苯酚发生酯化反应生成
,D和苯酚发生酯化反应生成 ,
,
(6)CH3CH2OH被催化氧化生成CH3CHO,CH3CHO和HCN发生加成反应生成CH3CH(OH)CN,该物质发生水解反应生成CH3CH(OH)COOH,以此解答该题.
解答 解:(1)由以上分析可知A为HCHO,B为 ,为苯乙醛,故答案为:HCHO;苯乙醛;
,为苯乙醛,故答案为:HCHO;苯乙醛;
(2)C结构简式为 ,C发生消去反应生成D,故答案为:消去反应;
,C发生消去反应生成D,故答案为:消去反应;
(3))①的反应的化学方程式为 ,为消去反应,反应条件为NaOH醇溶液、加热,
,为消去反应,反应条件为NaOH醇溶液、加热,
故答案为:NaOH醇溶液、加热;
(4)C发生缩聚反应生成E,E结构简式为 ,则③的反应的化学方程式为 n
,则③的反应的化学方程式为 n $→_{△}^{催化剂}$
$→_{△}^{催化剂}$ +nH2O,
+nH2O,
故答案为:n $→_{△}^{催化剂}$
$→_{△}^{催化剂}$ +nH2O;
+nH2O;
(5)D结构简式为 ,与D互为同分异构体且含有碳碳双键的苯的二取代物,其取代基为-CH=CH2、-COOH,有邻间对三种,如果取代基为-CH=CH2和HCOO-,有邻间对三种,所以符合条件的有6种,其中核磁共振氢谱为5组峰,且峰面积比为2:1:2:2:1的结构简式是
,与D互为同分异构体且含有碳碳双键的苯的二取代物,其取代基为-CH=CH2、-COOH,有邻间对三种,如果取代基为-CH=CH2和HCOO-,有邻间对三种,所以符合条件的有6种,其中核磁共振氢谱为5组峰,且峰面积比为2:1:2:2:1的结构简式是 ,
,
故答案为:6; ;
;
(6)CH3CH2OH被催化氧化生成CH3CHO,CH3CHO和HCN发生加成反应生成CH3CH(OH)CN,该物质发生水解反应生成CH3CH(OH)COOH,其合成路线为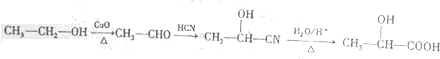 ,
,
故答案为: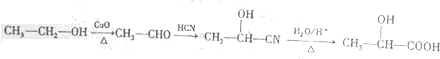 .
.
点评 本题考查有机物推断和有机合成,为高频考点,侧重考查学生分析推断及知识综合应用能力,明确有机物官能团及其性质、有机反应类型及反应条件是解本题关键,难点是根据反应物和生成物采用知识迁移的方法进行有机合成,题目难度中等.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
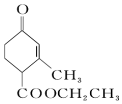 和
和  ,前者不含氧的官能团为(写结构简式)羰基、酯基,后者官能团有(写名称)酯基、羟基;
,前者不含氧的官能团为(写结构简式)羰基、酯基,后者官能团有(写名称)酯基、羟基;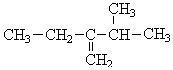 的名称为3-甲基-2-乙基-1-丁烯,
的名称为3-甲基-2-乙基-1-丁烯,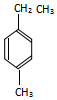 的名称为对甲基乙苯;
的名称为对甲基乙苯;
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
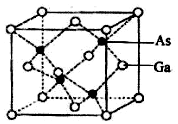 氮、磷、砷、钛的单质及其化合物在生产生活中有重要的应用.回答下列问题:
氮、磷、砷、钛的单质及其化合物在生产生活中有重要的应用.回答下列问题: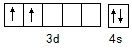 ,含Ti3+的配合物的化学式为[TiCl(H2O)5]Cl2•H2O,其配离子中含有的化学键类型为极性共价键、配位键,该配离子的配位数为6.
,含Ti3+的配合物的化学式为[TiCl(H2O)5]Cl2•H2O,其配离子中含有的化学键类型为极性共价键、配位键,该配离子的配位数为6.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用萃取的方法分离汽油和煤油 | |
| B. | 用NaOH溶液除去二氧化碳中的一氧化碳气体 | |
| C. | 加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铁粉 | |
| D. | 要鉴别水中是否有氯离子,可加入AgNO3溶液,观察是否产生白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在2L恒容密闭容器中,发生反应 2NO(g)+O2(g)?2NO2(g).
在2L恒容密闭容器中,发生反应 2NO(g)+O2(g)?2NO2(g).| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.007 | 0.006 | 0.006 | 0.006 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W、X、Y、Z最外层电子数之和为20 | B. | WX2、YX2和ZX2均只含共价键 | ||
| C. | 原子半径的大小顺序为X<W<Y<Z | D. | Z的气态氢化物比Y的稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com