
����Ŀ���¶�ΪTʱ����2.0 L�����ܱ������г���2.0 mol X����ӦX(g) ![]() Y(g)��Z(g)��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
Y(g)��Z(g)��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
t/s | 0 | 50 | 150 | 250 | 350 |
n(Y)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
����˵������ȷ����
A. ��Ӧ��ǰ250 s��ƽ������Ϊv(Y)��0.000 8 mol��L��1��s��1
B. ���������������䣬�����¶ȣ�ƽ��ʱc(Y)��0.21 mol��L��1����Ӧ����H>0
C. ��ͬ�¶��£���ʼʱ�������г���4.0 mol Y��4.0 mol Z���ﵽƽ��ʱ����˷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ1/20
D. ��ͬ�¶��£�����ʼʱ�������г���2.0 mol X��0.40 mol Y��0.80 mol Z����ﵽƽ��ǰv(��)>v(��)
 ��ǰ����ϵ�д�
��ǰ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ��п��ϡ������ɵ�ԭ����У�ͭ������������Ӧ���缫��Ӧʽ����п������������Ӧ���缫��Ӧʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��W��X��Y��Z��Q��ԭ��������������c��d��e��f��h������ЩԪ����ɵĶ�Ԫ�������Ȼ����Ӳ�����ĵ��ʺ�a����X��ɣ�b��W��Y��Q����Ԫ�����0.05mol/Lb��Һ��pHΪ1��d��ʹƷ����Һ��ɫ��e��Һ�壬f����ɫ��ӦΪ��ɫ���������ʵ�ת����ϵ��ͼ��ʾ(���������ȥ)������˵��������ǣ� ��
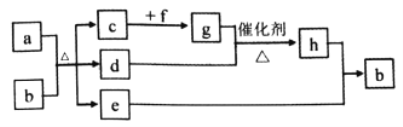
A. ��Ԫ������е㣺e>d>c B. �⻯����ȶ��ԣ�Q>Y>X
C. Ԫ�صķǽ����ԣ�Y>X>W D. ԭ�Ӱ뾶�Ĵ�С��Z>Q>Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ����Ҫ�Ĺ���Ԫ�أ�������ƻ������������Ҫ���ϣ������ƾ���(Na2MoO4��2H2O)��һ����Ҫ�Ľ�����ʴ����ij�����������(��Ҫ�ɷ�MoS2)Ϊԭ��ұ��������������ƾ������Ҫ����ͼ���£�
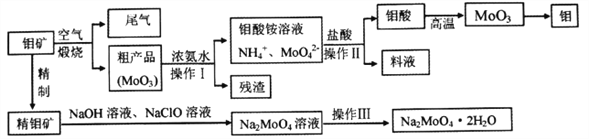
��1��Na2MoO4��2H2O��Ԫ�صļ�̬Ϊ_________����ҵ��������β���ù����İ�ˮ��������Ӧ�����ӷ���ʽΪ________________________________________________��
��2����ͼ����Ϣ�����ж�MoO3��____________�����(������������������������������)
��3������ NaClO���������ķ�������ʯ�е���������ù��̷��ȣ��仯ѧ��ӦΪ��NaClO+MoS2+NaOH��Na2MoO4+Na2SO4+NaCl+H2O���÷�Ӧ��ƽ�� NaClO��MoS2��ϵ����Ϊ____________�������¶����ߣ���Ľ����ʵı仯��ͼ������50��������ʽ��͵Ŀ���ԭ����____________________________________(д����)��
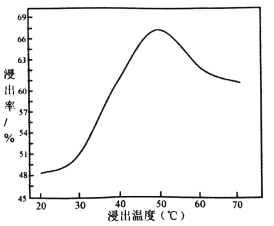
��4����������Ҫ����____________�����������õ�����Ҫˮϴ�����������Ƿ�ϴ�Ӹɾ��ķ�����____________________________________��
��5��﮺�MoS2�ɳ���صĹ���ԭ��ΪxLi+nMoS2![]() Li(MoS2)n�����س��ʱ�����ϵĵ缫��ӦʽΪ______________________��
Li(MoS2)n�����س��ʱ�����ϵĵ缫��ӦʽΪ______________________��
��6��ij������1.00��103�ִ����(��MoS216.00%)�Ʊ��ⵥ�ʣ���֪ұ�������У���������Ϊ10.00%�������յõ��ⵥ������Ϊ___________�֡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ϱ���������ͭ����NO2��Ӧ��ijС�����������ʵ��װ�ý���̽����̽���������ijɷ֣����������N2����NO��
��֪������KMnO4��Һ������NO����NO3����
NO��FeSO4��Һ��Ӧ��NO+FeSO4=[Fe(NO)]SO4(��ɫ)��
Cu2O+2H+=Cu+Cu2++H2O
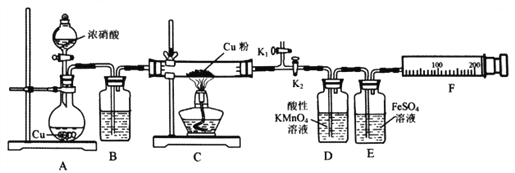
��ش��������⣺
��1��A�з�Ӧ�Ļ�ѧ����ʽΪ________________________��
��2�����װ�������ԣ�װ��ҩƷ��Ȼ��ʵ�����ȷ����˳����____________
���ر�K1����K2 ����Һ©������
����K1���ر�K2 ����ȼC���ƾ���
��3��ʵ������У�Dװ���е�������____________���ܷ����Dװ���е�����ȷ��C������NO����? ______��������________________________��
��4��Eװ�õ�������____________��
��5����ͭ����ȫ��Ӧ��ʵ��С��Է�Ӧ��Ĺ���ɷ�������²��룺��ֻ��CuO����ֻ��Cu2O����ͬѧ��Ϊ��ͨ���Ķ���ʵ�鼴���жϲ������Ƿ��������ʵ�鷽����_____________________��
��6��ʵ����Eװ����ʼ����δ����ɫ��С�����ͨ������ʵ��õ��������ݡ�
Cװ������ | Fװ����������(������Ϊ��״��) | ||
�������� | Cu���� | ��Ӧ��(����+������) | |
mg | 1.92g | (m+2.24)g | 112mL |
�ݴ�д��ʵ��ʱʵ�ʷ�����Ӧ�Ļ�ѧ����ʽ________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ö��Ե缫��ⷨ�Ʊ�����[H3BO3��B(OH) 3]�Ĺ���ԭ����ͼ��ʾ(��Ĥ����Ĥ�ֱ�ֻ���������Ӻ�������ͨ��)�������й�˵����ȷ���ǣ� ��

A. �������������������������Ϊ1��2 B. b���ĵ缫��ӦʽΪ2H2O��2e��=O2��+4H+
C. ��Ʒ���з����ķ�Ӧ��B(OH)3+OH��=B(OH)4�� D. ÿ����1 mol H3BO3��Ʒ��NaOH��Һ����22g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������֤�����������̼������Ӧ����ȷ��������װ����ͼ��ʾ(��֪��PdC12��Һ��CO�ܲ�����ɫ��Pd)������˵���������

A. װ�âٵ�������������ȡH2��NH3������
B. װ�â���ʯ��ˮ����Ǻ��ٵ�ȼ�ƾ���
C. װ�âڢ��зֱ�ʢװ����Na2CO3��Һ��ŨH2SO4
D. װ�â����к�ɫ�����������ķ�Ӧ��PdC12+CO+H2O=Pd��+CO2+2HC1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����373 Kʱ����0.5 mol N2O4ͨ�����Ϊ5 L�ĺ�������ܱ������У��������ֺ���ɫ���塣��Ӧ���е�2 sʱ��NO2��Ũ��Ϊ0.02 mol��L-1����60 sʱ����ϵ�ﵽƽ��״̬����ʱ�����ڵ�ѹǿΪ��ʼʱ��1.6��������˵��������ǣ� ��
A. ǰ2 s��N2O4��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ0.005 mol��L-1��s-1
B. ��2 sʱ��ϵ�ڵ�ѹǿΪ��ʼʱ��1.1��
C. ƽ��ʱ��ϵ�ں�N2O4 0.2 mol
D. ƽ��ʱ��N2O4��ת����Ϊ40%
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com