
| A.32 | B.120 | C.150 | D.180 |
科目:高中化学 来源:不详 题型:单选题
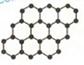
| A.石墨烯与石墨互为同位素 |
| B.0.12g石墨烯中含有6. 02×1022个碳原子 |
| C.石墨烯是一种有机物 |
| D.石墨烯中的碳原子间以共价键结合 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 物质 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 熔点/℃ | 2 852 | 2 072 | 714 | 190(2.6×105Pa) |
| 沸点/℃ | 3 600 | 2 980 | 1 412 | 182.7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氮化硅是分子晶体 |
| B.氮化硅是原子晶体 |
| C.氮化硅是离子晶体 |
| D.氮化硅化学式为Si4N3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
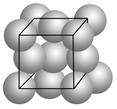
科目:高中化学 来源:不详 题型:单选题
| A.破损的晶体能够在固态时自动变成规则的多面体 |
| B.缺角的氯化钠晶体在饱和的NaCl溶液中慢慢变为完美的立方块 |
| C.圆形容器中结出的冰是圆形的 |
| D.由玻璃制成的圆形的玻璃球 |
查看答案和解析>>
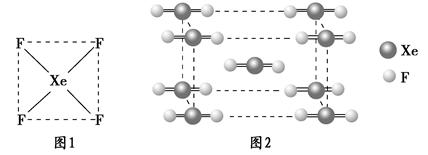
科目:高中化学 来源:不详 题型:单选题

| A.ZXY3 | B.ZX2Y6 | C.ZX4Y8 | D.ZX8Y12 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.CS2为V形的极性分子 |
B.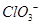 的空间构型为平面三角形 的空间构型为平面三角形 |
| C.SF6中有6对完全相同的成键电子对 |
D.SiF4和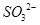 的中心原子均为sp3杂化 的中心原子均为sp3杂化 |
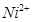 和
和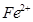 的离子半径分别为69pm和78pm,则熔点NiO_________________FeO(填“<”或“>”);
的离子半径分别为69pm和78pm,则熔点NiO_________________FeO(填“<”或“>”);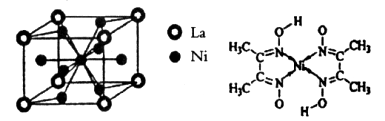
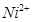 :在稀氨水介质中,丁二酮肟与
:在稀氨水介质中,丁二酮肟与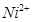 反应可生成鲜红色沉淀,其结构如右上图所示。
反应可生成鲜红色沉淀,其结构如右上图所示。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com