
36.5g HCl溶解在1L水中,所得溶液的密度为ρ g•mL﹣1,质量分数为w,物质的量浓度为cmol•L﹣1,NA表示阿伏加德罗常数,则下列叙述正确的是()
A. 所得溶液的物质的量浓度:c=1mol•L﹣1
B. 所得溶液中含有NA个HCl分子
C. 36.5g HCl气体在标准状况下占有的体积约为22.4L
D. 所得溶液的质量分数:w=36.5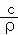
考点: 阿伏加德罗常数.
专题: 阿伏加德罗常数和阿伏加德罗定律.
分析: A.氯化氢溶于1L水中,所得溶液的体积不是1L;
B.氯化氢为强电解质,溶液中不存在氯化氢分子;
C.根据标准状况下的气体摩尔体积计算出氯化氢的体积;
D.根据物质的量浓度c=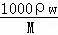 进行计算该溶液的质量分数.
进行计算该溶液的质量分数.
解答: 解:A.36.5g HCl的物质的量为1mol,1mol氯化氢溶解在1L水中,所得溶液体积不是1L,浓度不是1mol/L,故A错误;
B.氯化氢为强电解质,溶液中完全电离出氢离子和氯离子,所以溶液中不存在氯化氢分子,故B错误;
C.36.5g HCl的物质的量为1mol,标准状况下1mol氯化氢的体积约为22.4L,故C正确;
D.根据c=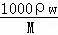 可得,w=
可得,w=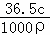 ,故D错误;
,故D错误;
故选C.
点评: 本题考查了有关物质的量的简单计算,题目难度不大,注意掌握物质的量与物质的量浓度、摩尔质量等物理量之间的转化关系,明确物质的量浓度与溶质质量分数的关系.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是( )
A.Na+、Ca2+、Cl-、SO42-B.Fe2+、H+、SO32-、ClO-
C.Mg2+、NH4+、Cl-、SO42-D.K+、Fe3+、NO3-、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
以葡萄糖为燃料的微生物燃料电池结构示意图如图所示.关于该电池的叙述正确的是()
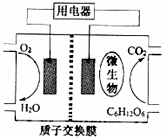
A. 该电池能够在高温下工作
B. 电池的负极反应为:C6H12O6+6H2O﹣24e﹣=6CO2↑+24H+
C. 放电过程中,H+从正极区向负极区迁移
D. 在电池反应中,每消耗1mol氧气,理论上能生成标准状况下CO2气体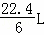
查看答案和解析>>
科目:高中化学 来源: 题型:
图表归纳是学习化学的一种常用方法,某同学表中归纳的内容与如图对应正确的是()
选项 x y z
A 胶体 混合物 淀粉溶液
B 化合物 酸性氧化物 一氧化氮
C 纯净物 化合物 液溴
D 强电解质 强酸 硫酸
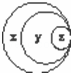
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理为2Fe(OH)3+3KClO+4KOH═2K2FeO4+3KCl+5H2O,下列说法正确的是()
A. 制备高铁酸钾用ClO﹣做还原剂
B. 制备高铁酸钾时1 mol Fe(OH)3得到3 mol 电子
C. 高铁酸钾中铁的化合价为+7
D. 用高铁酸钾处理水时,其还原产物能水解产生具有强吸附能力的胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氨基锂(Li2NH)是一种储氢容量高,安全性好的固体储氢材料,其储氢原理可表示为Li2NH+H2=LiNH2+LiH.下列有关说法正确的是()
A. Li2NH中N的化合价是﹣1
B. 该反应中H2既是氧化剂又是还原剂
C. Li+和H+的离子半径相等
D. 此法储氢和钢瓶储氢的原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
高锰酸钾在不同的条件下发生的反应如下:
MnO4﹣+5e﹣+8H+═Mn2++4H2O①
MnO4﹣+3e﹣+2H2O═MnO2↓+4OH﹣②
MnO4﹣+e﹣═MnO42﹣(溶液绿色)③
(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的酸碱性影响.
(2)将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为 ﹣→ +.
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色.下列说法正确的
a.氧化性:PbO2>KMnO4
b.还原性:PbO2>KMnO4
c.该反应可以用盐酸酸化
(4)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量之比为3:2,完成下列化学方程式(横线上填系数,括号内填物质):
KMnO4+ K2S+ KOH═ K2MnO4+3K2SO4+2S↓+ .
②若生成6.4g单质硫,反应过程中转移电子的物质的量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应属于加成反应的是()
A. CH2=CH2+HBr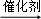 CH3CH2Br
CH3CH2Br
B. 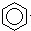 +Br2
+Br2
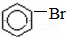 +HBr
+HBr
C. 2CH3CH2OH+O2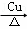 2CH3CHO+2H2O
2CH3CHO+2H2O
D. CH4+2Cl2 CH2Cl2+2HCl
CH2Cl2+2HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列短周期元素性质的数据:
元素编号
元素性质 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧
原子半径 0.74 1.60 1.52 1.10 0.99 1.86 0.75 0.82
最高或最低化合价 +2 +1 +5 +7 +1 +5 +3
﹣2 ﹣3 ﹣1 ﹣3
下列说法正确的是()
A. 原子序数④元素大于⑦元素
B. ②、③处于同一周期
C. 上述八种元素最高价氧化物对应的水化物,⑤号酸性最强
D. ⑧号元素原子结构示意图为:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com