
分析 该原电池中,Zn易失电子作负极、二氧化锰作正极,正极上二氧化锰得电子发生还原反应,负极上锌失电子发生氧化反应,在得失电子相同条件下正负极电极反应式相加即得电池反应式.
解答 解:该原电池中,Zn易失电子作负极、二氧化锰作正极,正极上二氧化锰得电子发生还原反应,电极反应式为MnO2+e-+H+=MnOOH;负极上锌失电子发生氧化反应,电极反应式为Zn-2e-=Zn2+;在得失电子相同条件下正负极电极反应式相加即得电池反应式,反应的离子方程式为Zn+2MnO2+2H+=Zn2++2MnOOH,
故答案为:MnO2+H++e-═MnOOH;2MnO2+Zn+2H+═2MnOOH+Zn2+.
点评 本题考查电极反应式的书写,为高频考点,明确各个电极上发生的反应是解本题关键,电极反应式的书写也是学习难点,题目难度中等.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 所得红棕色液体为氢氧化铁胶体 | |
| B. | 向该液体中逐滴加盐酸,开始时产生沉淀,盐酸足量时,沉淀消失 | |
| C. | 该液体含分散质微粒0.1 mol | |
| D. | 该液体具有丁达尔现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO3与BaCl2溶液作用,有白色沉淀生成,加稀HNO3后沉淀消失 | |
| B. | 将SO2气体分别通入Ba(OH)2溶液、FeCl3与BaCl2的混合溶液、HNO3酸化的BaCl2溶液中,均可有白色沉淀生成 | |
| C. | 将SO2气体通入BaCl2溶液中没有白色沉淀生成,将SO2气体通入Ba(NO3)2溶液中有白色沉淀生成 | |
| D. | 将SO2气体、Cl2一起通入BaCl2溶液中,或将SO2气体、NO2气体一起通入BaCl2 溶液中,均有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玻璃、水泥、水晶项链都是硅酸盐制品 | |
| B. | 晶体硅是在通信工程中制作光导纤维的主要原料 | |
| C. | 碳酸钠在医疗上是治疗胃酸过多的一种药剂 | |
| D. | 发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氯水呈浅黄色,且有刺激性气味,说明有Cl2分子存在 | |
| B. | 加入有色布条后,有色布条褪色,说明有HClO分子存在 | |
| C. | 加入含有NaOH的酚酞试液,红色褪去,说明有H+离子存在 | |
| D. | 加入盐酸酸化的AgNO3溶液产生白色沉淀,说明有Cl-离子存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
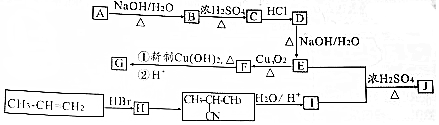
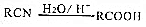
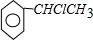 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$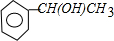 +NaCl;
+NaCl;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对平衡体系H2(g)+I2(g)?2HI(g)加压后,混合气体的颜色加深 | |
| B. | 用稀盐酸洗涤AgCl沉淀比用等体积的蒸馏水洗涤损失的AgCl少 | |
| C. | 实验室可用排饱和食盐水是方法收集氯气 | |
| D. | 工业合成三氧化硫的过程中使用过量的氧气,以提高二氧化硫的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com