
 主族 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | E | | F | | |
| 3 | A | C | D | | | | G | R |
| 4 | B | | | | | | H | |
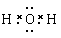 ; HCl>HBr。 (5) NaBr;
; HCl>HBr。 (5) NaBr;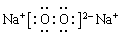 。
。 ;(7) ⅤA ; MH3。
;(7) ⅤA ; MH3。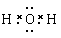 。同一主族的元素,元素的非金属性越强,对应的氢化物的稳定性就越强。由于Cl、Br是同一主族的元素,由于非金属性Cl>Br.所以氢化物的稳定性HCl>HBr。(5)Br元素跟Na元素形成的化合物的化学式是NaBr,Na2O2的电子式是
。同一主族的元素,元素的非金属性越强,对应的氢化物的稳定性就越强。由于Cl、Br是同一主族的元素,由于非金属性Cl>Br.所以氢化物的稳定性HCl>HBr。(5)Br元素跟Na元素形成的化合物的化学式是NaBr,Na2O2的电子式是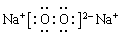 .(6)K和O两种元素形成的2:1型化合物K2O属于离子化合物,用电子式表示其形成过程为
.(6)K和O两种元素形成的2:1型化合物K2O属于离子化合物,用电子式表示其形成过程为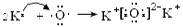 。(7) 按这个规定,第15列元素应为ⅤA ;由于其最外层有5个电子,要达到8的电子的稳定结构少三个电子,所以其简单氢化物的化学式为MH3。
。(7) 按这个规定,第15列元素应为ⅤA ;由于其最外层有5个电子,要达到8的电子的稳定结构少三个电子,所以其简单氢化物的化学式为MH3。

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.a-3=c+2 | B.质子数a>b>c>d |
| C.离子的还原性Y2-<Z- | D.离子半径X+< W3+< Y2-< Z- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.砹(85号元素)是一种有色固体,HAt应该不稳定,且AgAt是有色难溶于水固体 |
| B.铍(Be)是一种金属,它的氧化物的水化物可能具有两性 |
| C.硫酸锶(SrSO4)是难溶于水和盐酸的的白色固体 |
| D.硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碱土金属元素是指ⅡA族的所有元素 |
| B.除第一周期外,其他周期均有18种元素 |
| C.过渡元素都是副族元素 |
| D.主族元素的原子,半径越大,越容易得到电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径Y>Z,离子半径Z—<M2+ |
| B.MX2与水发生反应时,MX2只做氧化剂 |
| C.X、Y形成的化合物既能与强酸反应又能与强碱反应 |
| D.MX2、MZ2两种化合物中,都含有离子键和共价键,且阳离子与阴离子个数比均为1:2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 元素 | 信息 |
| X | K层电子数是L层电子数的2倍 |
| Y | 一种核素在考古时常用来鉴定一些文物的年代 |
| Z | 所处的周期序数与族序数相等 |
| W | 最高价氧化物对应的水化物酸性最强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com