
【题目】下列说法正确的是( )
A.CO、SO2均属酸性氧化物
B.凡能电离出H+的化合物均属于酸
C.碱性氧化物一定是金属氧化物
D.电解质可以是化合物,也可以是单质
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】I.下图是中学化学常用的实验装置,诮回答下列问题

(1)用图I进行物质的分离提纯,该分离方法为________,若利用装置I分离酒精和水的混合物,还缺少的仪器__________;①的名称是__________,②的进水口是________(填“f" 或“g”)。
(2)现需配制500mL、0.1mol/LKCl 溶液,装置Ⅱ是某同学转移溶液的示意图,指出图中的错误之处: ①_________;②____________。
(3)仪器①~④中,使用时必须检查是否漏水的是_________(填序号)。
Ⅱ.分离和提纯物质的方法不仅用于实验研究而且广泛应用于工业生产和生活实际。
(4)海水晒盐过程中,通过蒸发的方法可得到粗盐固体;再将粗盐固体溶解后,再用过滤的方法除去其中的泥沙。粗盐中除泥沙外还含有可溶性杂质(如下表所示),可按下表所示由上至下的顺序依次除去(将表格填写完整)。
杂质 | 加入试剂的化学式 | 发生反应的离子方程式 |
硫酸盐 | ___________ | ___________ |
MgCl2 | NaOH | ___________ |
CaCl2 | Na2CO3 | ___________ |
依次加入上述试剂后,完全反应后,再进行过滤,再加入适量的盐酸 可除去上述步骤引入的 杂质离子。
(5) 从海带中可提取碘单质。用萃取的方法可将碘单质从水溶液中提取出来,该方法利用了I2在不同溶剂中的_______性不同。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列九种物质:①H2O,②Al,③CO2,④盐酸,⑤硫酸钡,⑥NaOH⑦饱和FeCl3溶液,⑧氨水,⑨乙醇。根据上述提供的物质,回答下列问题:
(1)属于电解质的是 _______________________(填序号),属于非电解质__________(填序号)。
(2)上述物质间发生的某反应的离子方程式为H++OH===H2O,则该反应的化学方程式为_________________________________________________________________________。
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________(填序号),反应的离子方程式为____________________________________________________________________________。
(4)Al和Na的单质同时加入到一定量的水中,充分反应后,发现既无沉淀生成又无固体残留物存在,请用两个离子方程式表示其变化:______________________________; ____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,与100 mL 0.5 mol/LCaCl2溶液所含的Cl-的物质的量浓度相同的是( )
A. 10 mL 0.5 mol/LMgCl2溶液 B. 100 mL 0. 5 mol/L HCl溶液
C. 500 mL 0.2 mol/L NaCl溶液 D. 1000 mL0.05 mol/L BaCl2 溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示。

(1)只根据图I、II所示实验,能够达到实验目的是(填装置序号)__________________;
(2)图III、IV所示实验均能鉴别这两种物质,与实验III相比,实验IV的优点是_________;(填选项序号)
A.IV比III复杂 B.IV比III安全
C.IV比III操作简便 D.IV可以做到用一套装置同时进行两个对比实验,而III不行
(3)若用实验IV验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是___________________;
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应。当碳酸氢钠溶液过量时,其离子方程式为__________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物含有C、H、O三种元素,其质谱如图所示.将4.3g该有机物在O2中充分燃烧,使生成物依次通过足量浓硫酸和碱石灰,浓硫酸增重2.7g,碱石灰增重8.8g,则: 
(1)该有机物的摩尔质量为 .
(2)该有机物的分子式为 .
(3)1mol该有机物与足量的金属钠反应产生1mol氢气,核磁共振氢谱有两个峰,且面积比为2:1,请写出其结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知烯烃与苯在一定条件下反应生成芳香烃,如: ![]() +H2C=CH2
+H2C=CH2 ![]()
![]()
![]() +2H2C=CH2
+2H2C=CH2 ![]()
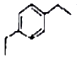
![]() +2H2C=CH2
+2H2C=CH2 ![]()
![]()
丙烯是三大合成材料的基本原料,可用于合成应用广泛的DAP树脂单体和双酚等有机物,具有重要的工业用途.
(1)写出丙烯在一定条件下发生聚合反应的化学方程式 .
(2)丙烯与苯在一定条件下反应可生成M、N等多种芳香烃.红外光谱、核磁共振是研究机物结构的重要方法,根据下列数据,写出M,N的结构简式. M:元素组成:C89.99%、H 10.06%;1H核磁共振有5个信号.
N:元素组成:C88.82%、H11.18%;1H核磁共振有3个信号.
M: , N: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、实验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O回答下列问题:
(1)该反应中被氧化的元素是__________.
(2)氧化性:KMnO4__________Cl2(填“>”、“<”或“=”)
(3)该反应中氧化剂和氧化产物的物质的量之比为__________.
(4)用双线桥法表示该反应中电子转移的方向和数目:_________
2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(5)每生成标准状况下2.24L Cl2,反应中转移电子的物质的量为__________.
Ⅱ、实验室常用以下方法制取氯气:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:
MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:
(1)把氯气通入紫色石蕊试液中,可以观察到的现象是:________________,请你解释其中的原因 __________________________________________________
(2)为保证实验安全,常用NaOH溶液吸收多余的氯气。写出反应的化学方程式__________________________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com