
氯气在298K、100kPa![]() 时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有三分之一与水反应。请回答下列问题:
时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有三分之一与水反应。请回答下列问题:
(1)该反应的离子方程式为__________;
(2)估算该反应的平衡常数__________(列式计算)
(3)在上述平衡体系中加入少量NaOH固体,平衡将向________移动;
(4)如果增大氯气的压强,氯气在水中的溶解度将______(填“增大”、“减小”或“不变”),平衡将向______________移动。
[答案](1)![]() ;
;
(2)![]() (水视为纯液体)
(水视为纯液体)
C起 0.09 0 0 0
C变 0.09×![]() 0.03 0.03 0.03
0.03 0.03 0.03
C平 0.06 0.03 0.03 0.03
![]() ;
;
(3)正反应方向;(4)增大,正反应方向
命题立意:平衡相关内容的综合考查
解析:题干中用“溶于水的Cl2约有三分之一与水反应”给出可逆反应![]() (该反应在教材中通常没提及可逆);平衡常数的计算根据题中要求列三行式求算;平衡移动是因为H+的减少向正反应方向移动;增大压强将增大氯气的浓度,平衡向正反应方向移动。
(该反应在教材中通常没提及可逆);平衡常数的计算根据题中要求列三行式求算;平衡移动是因为H+的减少向正反应方向移动;增大压强将增大氯气的浓度,平衡向正反应方向移动。
【技巧点拨】平衡题在近年的高考题中比较平和,但新课标高考题今年引入了对过程呈现的考查,这是以后高考中应注意的。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
| 实验 | 外加试剂 | 现象 |
| A | 1滴0.2mol/LNaOH溶液 | 不变色 |
| B | 1滴水 | 缓慢变浅棕褐色 |
| C | 1滴0.1mol/L硫酸 | 迅速变棕褐色 |
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖北省高三上学期12月月考化学试卷(解析版) 题型:选择题
氯气在298K、100kPa时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有三分之一与水反应。估算该反应的平衡常数( )
A.4.5×10-4 B.0.015 C.5.4×10-5 D.无法计算
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江西省高三12月月考理综考化学试卷(解析版) 题型:选择题
氯气在298K、101kPa时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有三分之一与水反应。估算该反应的平衡常数( )
A.5.4×10—5 B.4.5×10—4 C.0.015 D.无法计算
查看答案和解析>>
科目:高中化学 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
(16分)镁化合物和氯气均具有广泛用途,请回答下列问题:
(1)写镁和氯气反应产物的电子式
(2)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。则下列选项中正确的是
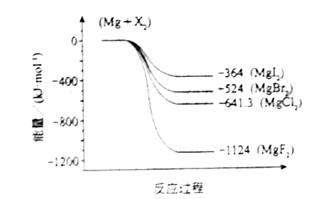
A MgI2中Mg2+与I-间的作用力小于MgF2中Mg2+与F-间的作用力
B Mg与X2的反应是放热反应
C MgBr2与Cl2反应的△H<0
D 化合物的热稳定性顺序为MgI2>MgBr2>MgCl2>MgF2
(3)在298K、100Kpa时,在1L水中可溶解0.09mol氯气,实验测得溶于水的Cl2约有三分之一与水反应。请回答下列问题:
① 该反应的离子方程式为 ,平衡常数表达式为
②在上述平衡体系中加入少量NaCl固体,平衡将 (填“正向移动”、“逆向移动”、“不移动”);增大氯气的压强,氯气的溶解度将 ,氯气和水反应的平衡常数将
(填“变大”、“变小”、“不变”)。
③已知:
H2CO3  HCO3- + H+
Ka1(H2CO3) = 4.45×10-7
HCO3- + H+
Ka1(H2CO3) = 4.45×10-7
HCO3- CO32- + H+
Ka2(H2CO3) = 5.61×10-11
CO32- + H+
Ka2(H2CO3) = 5.61×10-11
HClO  H+ + ClO-
Ka(HClO) = 2.95×10-8
H+ + ClO-
Ka(HClO) = 2.95×10-8
请依据以上碳酸和次氯酸的电离平衡常数,写出在下列条件下所发生反应的离子方程式:
将少量的氯气通入到过量的碳酸钠溶液中____________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
氯气在298K、100kPa![]() 时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有三分之一与水反应。估算该反应的平衡常数( )
时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有三分之一与水反应。估算该反应的平衡常数( )
A.4.5×10-4 B.0.015 C.5.4×10-5 D.无法计算
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com