
(17分)运用化学反应原理研究溶液的组成与性质具有重要意义。请回答下列问题:
(1)用惰性电极电解含有NaHCO3的NaCl溶液,假设电解过程中产生的气体全部逸出,测得溶液pH变化如图所示。
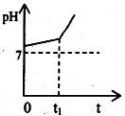
则在0→t1时间内,阳极反应式为 ,溶液pH升高比较缓慢的原因是(用离子方程式回答) 。
(2)含氨废水易引发水体富营养化。向NH4Cl溶液中加入少量NaOH固体,
溶液中 ______________(填“增大”“减小”或“不变);25℃时,NH3·H2O的电离平衡常数Kb=1.8×10—5mol·L—1,该温度下,1 mol·L—1的NH4Cl溶液中c(H+)=________________ mol
______________(填“增大”“减小”或“不变);25℃时,NH3·H2O的电离平衡常数Kb=1.8×10—5mol·L—1,该温度下,1 mol·L—1的NH4Cl溶液中c(H+)=________________ mol L
L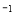 。(已知
。(已知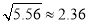 )
)
(3)如果粗盐中SO42-含量较高,精制过程需添加钡试剂除去SO42-,该钡试剂可选用下列试剂中的 。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
现代工艺中更多使用BaCO3除SO42-,请写出发生反应的离子方程式 。
(4)某工业生产中,向含有大量Ca2+、Mn2+的溶液中加入足量NH4HCO3,生成MnCO3沉淀和CO2,写出该反应的离子方程式 ,剩余溶液中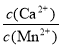 < 。
< 。
[已知Ksp(MnCO3)=1×10-11(mol·L-1)2,Ksp(CaCO3)=5 ×10-9(mol·L-1)2]
(1)2Cl--2e-=Cl2↑ (2分) HCO3- + OH- = CO32- + H2O (2分)
(2)不变(2分) 2.36x10-5 (3分)
(3) a、c (2分) BaCO3(s)+ SO42-(aq)= BaSO4(s)+ CO32-(aq)(2分)
(4) Mn2+ +2 HCO3- = MnCO3↓+ CO2↑+ H2O (2分) 500 (2分)
【解析】
试题分析:(1)用惰性电极电解NaHCO3和NaCl的混合溶液时,反应过程分两段进行,第一段:相当于电解氯化钠溶液,阳极上氯离子放电,阴极上氢离子放电,同时生成氢氧化钠,氢氧化钠和碳酸氢钠反应生成碳酸钠和水;第二段电【解析】
当氯离子完全析出后,相当于电解碳酸氢钠和碳酸钠的混合液,阳极上氢氧根离子放电,阴极上氢离子放电,实际上相当于电解水。故在0→t1时间内,相当于电解氯化钠溶液,阳极上氯离子放电,电极反应式为2Cl--2e-═Cl2↑,阴极上氢离子放电,电极反应式为:2H++2e-═H2↑,溶液中还有氢氧化钠生成,氢氧化钠和碳酸氢钠反应生成碳酸钠,离子反应方程式为OH-+HCO3-═H2O+CO32-,所以溶液pH升高比较缓慢;(2) 为NH4+水解平衡常数的倒数,NH4Cl溶液中加入少量NaOH,平衡常数不变,则该比值不变;根据盐类的水解与弱电解质电离的关系,水解平衡常数Kh=Kw/Kb=1.0×10-14÷1.8×10-5=5.56×10-10mol?L?1,则c(NH3?H2O)?c(H+)/c(NH4+)=5.56×10-10mol?L?1,因为c(NH3?H2O)≈c(H+),c(NH4+)≈1mol?L?1,带入计算式可得c(H+)=2.36×10-5mol?L?1。(3)Ba(OH)2可与SO42?反应,OH?可加盐酸除去,BaCl2可与SO42?反应,而且不引入新杂质,Ba(NO3)2能与SO42?反应,但NO3?无法除去,选ac;BaCO3转化为更难溶的BaSO4,离子方程式为:BaCO3(s) + SO42-(aq) = BaSO4 (s) + CO3 2-(aq)。(4)向含有大量Ca2+、Mn2+的溶液中加入足量NH4HCO3,生成MnCO3沉淀和CO2,该反应的离子方程式Mn2++2HCO3- = MnCO3↓+ CO2↑+ H2O,剩余溶液中无沉淀,根据沉淀溶解平衡知识溶度积规则知,Q<Ksp,则剩余溶液中
为NH4+水解平衡常数的倒数,NH4Cl溶液中加入少量NaOH,平衡常数不变,则该比值不变;根据盐类的水解与弱电解质电离的关系,水解平衡常数Kh=Kw/Kb=1.0×10-14÷1.8×10-5=5.56×10-10mol?L?1,则c(NH3?H2O)?c(H+)/c(NH4+)=5.56×10-10mol?L?1,因为c(NH3?H2O)≈c(H+),c(NH4+)≈1mol?L?1,带入计算式可得c(H+)=2.36×10-5mol?L?1。(3)Ba(OH)2可与SO42?反应,OH?可加盐酸除去,BaCl2可与SO42?反应,而且不引入新杂质,Ba(NO3)2能与SO42?反应,但NO3?无法除去,选ac;BaCO3转化为更难溶的BaSO4,离子方程式为:BaCO3(s) + SO42-(aq) = BaSO4 (s) + CO3 2-(aq)。(4)向含有大量Ca2+、Mn2+的溶液中加入足量NH4HCO3,生成MnCO3沉淀和CO2,该反应的离子方程式Mn2++2HCO3- = MnCO3↓+ CO2↑+ H2O,剩余溶液中无沉淀,根据沉淀溶解平衡知识溶度积规则知,Q<Ksp,则剩余溶液中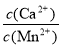 < Ksp(CaCO3)/ Ksp(MnCO3)=500。
< Ksp(CaCO3)/ Ksp(MnCO3)=500。
考点:考查电解原理,盐类的水解和沉淀溶解平衡。


科目:高中化学 来源:2014-2015学年陕西省西安市高三上学期阶段四考试化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.配制0.1mol/L H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释
B.实验室制备Cl2,可用排饱和食盐水集气法收集
C.实验室中,钠通常保存在盛有煤油的细口瓶中
D.定容时仰视容量瓶刻度线,所配制的NaOH溶液浓度将偏高
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省宝鸡市高一上学期期末化学试卷(解析版) 题型:填空题
冶炼金属常用以下几种方法:①以C、CO或H2做还原剂 ②以活泼金属Na、Mg等还原 ③利用铝热反应原理还原 ④电解法 ⑤热分解法。下列金属各采用哪种方法还原最佳。(用序号填写下列空白。)
(1)Fe、Zn、Cu等中等活泼金属 。
(2)Na、Mg、Al等活泼或较活泼金属 。
(3)Hg、Ag等不活泼金属 。
(4)V、Cr、Mn、W等高熔点金属 。
(5)K、Rb、Cs、Ti等金属通常还原方法是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省宝鸡市高一上学期期末化学试卷(解析版) 题型:选择题
下列反应中能检验尿液中存在葡萄糖的是
A.加金属钠,看是否有氢气放出
B.与新制的Cu(OH)2悬浊液混合煮沸,观察有无红色沉淀生成
C.与醋酸和浓硫酸共热,看能否发生酯化反应
D.加入饱和碳酸钠溶液中看是否分层
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省枣庄市高三1月月考理综化学试卷(解析版) 题型:选择题
下列实验操作的叙述不正确的是:
A.中和滴定时,锥形瓶不用润洗
B.用试纸检验气体性质时,需先将试纸湿润,再检验
C.FeBr2溶液中通入少量Cl2,再加入CCl4,CCl4层不变色
D.向盐酸酸化的Ba(NO3)2溶液中通入SO2,不会产生沉淀
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期12月月考化学试卷(解析版) 题型:填空题
(14分)某工业废水中含有CN-和Cr2O72—等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理:

回答下列问题:
(1)步骤②中,CN-被ClO-氧化为CNO-的离子方程式为________________。
(2)步骤③的反应为S2O32—+ Cr2O72—+H+ SO42—+Cr3++H2O(未配平),则每消耗0.4mol Cr2O72—转移__________mol e-。
SO42—+Cr3++H2O(未配平),则每消耗0.4mol Cr2O72—转移__________mol e-。
(3)含Cr3+废水可以加入熟石灰进一步处理,目的是____________________。
(4)在25℃下,将amol·L—1的NaCN溶液与0.01mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,用含a的代数式表示HCN的电离常数Ka=_________________。若25?C 时Ka=1×10-9 则同体积均为0.1mol·L-1的NaCN、HCN的混合溶液中下列说法不正确的是
a.此溶液一定有C(Na+)+C(H+)=C(OH?)+C(CN?)
b.混合溶液中水的电离程度一定大于该温度下纯水的电离程度。
c.此溶液一定有C(Na+)=C(HCN)+ C(CN?)
d.此溶液加入少量氢氧化钠或盐酸溶液的PH值变化不大
(5)取工业废水水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀。该过程中反应的离子方程是____________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴彦淖尔市高三上学期期中考试化学试卷(解析版) 题型:填空题
(10分)短周期中五种元素A、B、C、D、E原子序数依次增大,其中A、B、C原子核外电子层数之和是5,且C原子最外层上的电子数为A和B两元素原子最外电子层上电子数的总和,C原子的价电子构型为nsnnpn+1,A原子的最外层电子数等于其电子层数。D和E可以形成原子个数比为1:1和1:2的两种离子化合物,且D原子的2p能级上有两个未成对电子,试回答下列问题:
(1)B、C、D、E四种元素的原子,半径从大到小的顺序是
(填元素符号或化学式,下同);第一电离能从大到小的顺序是
(2)由A、C两种元素形成的离子化合物中C元素的质量分数为73.68%,它的所有原子最外层都符合相应的稀有气体原子的最外层电子层结构,该物质加热时就能分解为两种气体,则X的化学式为 ,X受热分解的化学方程式为_____________________ 。
(3)C和E形成一种离子化合物Y,其摩尔质量为65 g/mol,Y受热或撞击时立即分解为两种单质。则Y的化学式为 ,Y的阴离子是一种弱酸根离子,全由C元素组成,与Y的阴离子具有相同原子数和电子数的分子有 (任写一种),Y与盐酸反应的离子方程式为 。
(4)(CA4)2SO4溶液加水稀释时,溶液中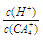 的值将 (填“增大”、“减少”或“不变”)。
的值将 (填“增大”、“减少”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、化合物 zeylastral可以发生水解反应 |
| B、能与FeCl3溶液、银氨溶液发生反应 |
| C、1mol zeylastral最多与5molH2发生反应 |
| D、1mol zeylastral最多可与2molBr2发生反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com