
| m | n | ||
| x | y |
·ÖĪö ÓÉĖÄÖÖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲŌŚÖÜĘŚ±ķÖŠĪ»ÖĆ£¬æÉÖŖm”¢n“¦ÓŚµŚ¶žÖÜĘŚ£¬x”¢y“¦ÓŚµŚČżÖÜĘŚ£¬ÉčnµÄŌ×ÓŠņŹżĪŖa£¬ŌņmŌ×ÓŠņŹżĪŖa-1£¬xŌ×ÓŠņŹżĪŖa+9£¬yµÄŌ×ÓŠņŹżĪŖa+10£¬ĖüĆĒµÄŌ×ÓŠņŹż×ÜŗĶĪŖ46£¬Ōņa-1+a+a+9+a+10=46£¬½āµĆa=7£¬ŌņnĪŖNŌŖĖŲ”¢mĪŖCŌŖĖŲ”¢xĪŖSŌŖĖŲ”¢yĪŖCl£®
½ā“š ½ā£ŗÓÉĖÄÖÖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲŌŚÖÜĘŚ±ķÖŠĪ»ÖĆ£¬æÉÖŖm”¢n“¦ÓŚµŚ¶žÖÜĘŚ£¬x”¢y“¦ÓŚµŚČżÖÜĘŚ£¬ÉčnµÄŌ×ÓŠņŹżĪŖa£¬ŌņmŌ×ÓŠņŹżĪŖa-1£¬xŌ×ÓŠņŹżĪŖa+9£¬yµÄŌ×ÓŠņŹżĪŖa+10£¬ĖüĆĒµÄŌ×ÓŠņŹż×ÜŗĶĪŖ46£¬Ōņa-1+a+a+9+a+10=46£¬½āµĆa=7£¬ŌņnĪŖNŌŖĖŲ”¢mĪŖCŌŖĖŲ”¢xĪŖSŌŖĖŲ”¢yĪŖCl£®
£Ø1£©ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬ŌŖĖŲnµÄŌ×ÓŠņŹżĪŖ7£¬¹Ź“š°øĪŖ£ŗ7£»
£Ø2£©xĪŖSŌŖĖŲ£¬Ō×ӵļŪµē×Ó½į¹¹ĪŖ3s23p4£¬¹Ź“š°øĪŖ£ŗ3s23p4£»
£Ø3£©mÓėyĖłŠĪ³É»ÆŗĻĪļµÄ»ÆѧŹ½ĪŖCCl4µČ£¬¹Ź“š°øĪŖ£ŗCCl4£»
£Ø4£©ClŌ×ÓµÄŗĖµēŗÉŹż±ČSµÄ“ó£¬Ō×Ó°ė¾¶±ČSµÄŠ”£¬¹ŹClµÄŌ×ÓŗĖĪüŅżµē×ÓµÄÄÜĮ¦±ČĮņµÄĒ棬¹ŹClµÄµēøŗŠŌ½Ļ“ó£¬
¹Ź“š°øĪŖ£ŗCl£»ClŌ×ÓµÄŗĖµēŗÉŹż±ČSµÄ“ó£¬Ō×Ó°ė¾¶±ČSµÄŠ”£¬¹ŹClµÄŌ×ÓŗĖĪüŅżµē×ÓµÄÄÜĮ¦±ČĮņµÄĒ森
µćĘĄ ±¾Ģāæ¼²é½į¹¹ŠŌÖŹĪ»ÖĆ¹ŲĻµÓ¦ÓĆ£¬×¢Ņā“Ó½į¹¹ÉĻĄķ½āµēøŗŠŌĒæČõ£¬×¢ŅāĄķ½āĶ¬Ö÷×åŌŖĖŲŌ×ÓŠņŹż¹ŲĻµ£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 A”¢B”¢C”¢D”¢E”¢XŹĒ֊ѧ³£¼ūµÄĪŽ»śĪļ£¬“ęŌŚČēĶ¼×Ŗ»Æ¹ŲĻµ£Ø²æ·ÖÉś³ÉĪļŗĶ·“Ó¦Ģõ¼žĀŌČ„£©£®
A”¢B”¢C”¢D”¢E”¢XŹĒ֊ѧ³£¼ūµÄĪŽ»śĪļ£¬“ęŌŚČēĶ¼×Ŗ»Æ¹ŲĻµ£Ø²æ·ÖÉś³ÉĪļŗĶ·“Ó¦Ģõ¼žĀŌČ„£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±½”¢¼×±½ | B£® | ŅŅČ²”¢±½ŅŅĻ© | C£® | ¼×Č©”¢¼×Ėį¼×õ„ | D£® | ŅŅĻ©”¢»·¼ŗĶé |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | øƶąėÄĖ®½ā²śĪļÖŠĪŽ | B£® | øƶąėÄŹĒŅ»øöĪåėÄ | ||
| C£® | øƶąėľßÓŠĮ½ŠŌ | D£® | øƶąėÄ·Ö×ÓÖŠÓŠĖÄøöėļü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | C£® |  | D£® | 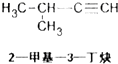 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗ¬ÓŠ½šŹōŌŖĖŲµÄ»ÆŗĻĪļŅ»¶ØŹĒĄė×Ó»ÆŗĻĪļ | |
| B£® | ¢ńA×åŗĶ¢÷A×åŌŖĖŲŌ×Ó»ÆŗĻŹ±£¬Ņ»¶ØŠĪ³ÉĄė×Ó¼ü | |
| C£® | ÓÉ·Ē½šŹōŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļŅ»¶ØŹĒ¹²¼Ū»ÆŗĻĪļ | |
| D£® | »īĘĆ½šŹōÓė»īĘĆ·Ē½šŹō»ÆŗĻŹ±£¬ÄÜŠĪ³ÉĄė×Ó¼ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆ½šŹōÄĘæÉĒų·ÖŅŅ“¼ŗĶŅŅĆŃ | |
| B£® | ÓĆäåĖ®æÉĒų·Ö¼ŗĶéŗĶ3--¼ŗĻ© | |
| C£® | ÓĆĖ®æÉĒų·Ö±½ŗĶäå±½ | |
| D£® | ÓĆŠĀÖʵÄĒāŃõ»ÆĶŠü×ĒŅŗæÉĒų·Ö¼×Ėį¼×õ„ŗĶŅŅČ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹŌ¹ÜæÉ×÷ĪŖ·“ӦȯĘ÷ | |
| B£® | ĮæĶ²ÓĆÓŚĮæČ”Ņ»¶ØŅŗĢåŅ©Ę· | |
| C£® | ½ŗĶ·µĪ¹ÜÓĆ¹żÓ¦Į¢¼“ĒåĻ“µĪĘæÖŠµÄµĪ¹ÜŅ²ŹĒČē“Ė | |
| D£® | ÉÕ±³£ÓĆ×÷ÅäÖĘČÜŅŗŗĶ½Ļ“óŹŌ¼ĮµÄ·“ӦȯĘ÷ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com