
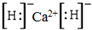 ��
������ ��1���⻯��Ϊ���ӻ�����ݴ���д����ʽ��
��2��S��Hg��Ӧ����HgS��
��3��������Ӧ��Ԫ�ػ��ϼ۱仯������������ԭ��Ӧ��ʧ�����غ㡢ԭ�Ӹ����غ���ƽ����ʽ��
��4�������������������������Ļ�ѧʽ��Ȼ����д���ɣ�
��� �⣺��1���⻯��Ϊ���ӻ������ʧȥ2�����Ӹ�Hԭ�ӣ��Ӷ��γ���H�����ӣ��ʴ�Ϊ��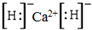 ��
��
��2��Hg��S��Ӧ����HgS����ѧ��Ӧ����ʽΪ��Hg+S=HgS���ʴ�Ϊ��Hg+S=HgS��
��3����Ӧ��ClԪ�ش�+4�۽���Ϊ-1�ۣ����������NԪ�ش�-3����Ϊ0�ۣ�C��+2�����ߵ�+4�ۣ�Ҫʹ��ʧ�����غ㣬�������ȷ���ϵ��Ϊ2���������ϵ��Ϊ2�����ݵ���غ�ó��Ⱥ�ǰ�����������ӣ�����ԭ�Ӹ����ó������ˮ���ʴ�Ϊ��2��2��4OH-��2��1��2��2H2O��
��4��SiO2��������������һ�ּ�ǿ�Ķ�Ԫ���ˮ��������3��Ԫ����ɣ����з�Ԫ�ص���������Ϊ79.17%��������Hԭ����ĿΪ2�������Ļ�ѧʽΪ��H2SixFy�����ݻ��ϼ۴�����Ϊ0��֪2+4x-y=0���ɷ�Ԫ������������$\frac{19y}{2+28x+19y}$=79.17%���������x=1��y=6���ʸ���ΪH2SiF6����SiO2�������������ӷ�Ӧ����ʽΪ��SiO2+6HF=2H++SiF62-+2H2O���ʴ�Ϊ��SiO2+6HF=2H++SiF62-+2H2O��
���� ������Ҫ������ǵ���ʽ����д�����ӷ�Ӧ����ʽ����д����ƽ����һ�����Ѷȣ�


 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
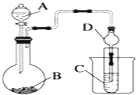 ij��ѧ��ȤС��Ϊ̽��Ԫ�����ʵĵݱ���ɣ����������ϵ��ʵ�飮
ij��ѧ��ȤС��Ϊ̽��Ԫ�����ʵĵݱ���ɣ����������ϵ��ʵ�飮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
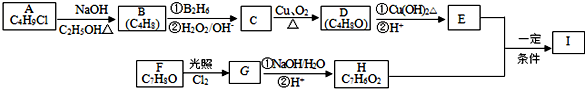
 ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ�����У�������ѹǿ�����SiCl4��ת���� | |
| B�� | ����Ӧ��ʼʱSiCl4Ϊ1 mol�����ƽ��ʱ����������ΪQ kJ | |
| C�� | ��Ӧ��4 minʱ����HClŨ��Ϊ0.12 mol/L����H2�ķ�Ӧ����Ϊ0.03 mol/��L•min�� | |
| D�� | ��Ӧ����0.025Q kJ����ʱ�����ɵ�HClͨ��100 mL 1 mol/L��NaOH��Һ��ǡ����ȫ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
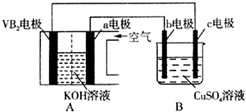 ��������VB2��-������ع���ʱ��ӦΪ��4VB2+11O2=4B2O3+2V2O5���øõ�ص��200mL����ͭ��Һ��ʵ��װ����ͼ��ʾ��b��c��Ϊ���Ե缫���������·��ͨ��0.04mol����ʱ��Bװ���������ռ���0.448L���壨��״����������˵����ȷ���ǣ�������
��������VB2��-������ع���ʱ��ӦΪ��4VB2+11O2=4B2O3+2V2O5���øõ�ص��200mL����ͭ��Һ��ʵ��װ����ͼ��ʾ��b��c��Ϊ���Ե缫���������·��ͨ��0.04mol����ʱ��Bװ���������ռ���0.448L���壨��״����������˵����ȷ���ǣ�������| A�� | �������У�b�缫�������к�ɫ����������Ȼ�������ݲ��� | |
| B�� | VB2Ϊ�������缫��ӦΪ��2VB2+11H2O-22e-=V2O5+2B2O3+22H+ | |
| C�� | ����ڲ�OH-����a�缫����ҺpH��С | |
| D�� | ������Һ����仯������Bװ������Һ��pHΪ1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ������� | �������� | ��ʼ���ʵ���/mol | ƽ��ʱSO3�����ʵ���/mol | ||
| SO2 | O2 | SO3 | |||
| �� | ���º��� | 2 | 1 | 0 | 1.2 |
| �� | ���Ⱥ��� | 0 | 0 | 2 | a |
| �� | ���º�ѹ | 2 | 1 | 0 | b |
| A�� | ƽ��ʱSO3�����ʵ�����a��1.2��b��1.2 | |
| B�� | ��������ƽ�ⳣ����ͬ | |
| C�� | ���� I��SO2��ת��������������SO3��ת����֮��С��1 | |
| D�� | ����ʼʱ���������г���1.0mol SO2 ��g����0.40mol O2��g����1.40mol SO3 ��g�������ʱ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 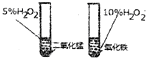 �Ƚ϶������̺�����þ�Ĵ�Ч�� | B�� | 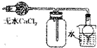 �����ռ����� | ||
| C�� | 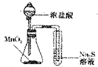 �Ƚ϶������̡���������������� | D�� |  �۲�����������ʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ̼ԭ������n�� | 6 | 8 | 10 | 12 | �� |
| �ṹ��ʽ | 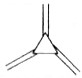 | 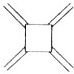 | 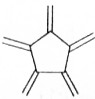 | 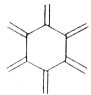 | �� |
| A�� | ��ϩ��ͨʽ�ɱ�ʾΪCnHn | |
| B�� | n=100����ϩ�����к���50��̼̼˫�� | |
| C�� | n=6����ϩ���ӵ�ͬ���칹���к�������̼̼�����Ľṹ��6�� | |
| D�� | n=8����ϩ���ӵ�ͬ���칹��������ڷ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �軯�أ�KCN�� | B�� | ��Ȳ��C2H2�� | C�� | ����泥�NH4CNO�� | D�� | ̼���裨SiC�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com