
| A.11 : 1 | B.12 : 11 | C.9 : 2 | D.9: 1 |
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.将煤液化、气化,提高燃料的燃烧效率 |
| B.在汽车上安装汽车尾气催化转化装置,使之发生反应: 2CO+2NO 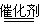 2CO2+N2 2CO2+N2 |
| C.在大力推广乙醇汽油的同时,研究开发太阳能汽车和氢氧燃料电池汽车 |
| D.在水力发电、火力发电、核能发电和风力发电中,要大力发展火力发电 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 2CrO42—+2H+平衡左移,导致Ag2CrO4沉淀过迟,影响实验结果
2CrO42—+2H+平衡左移,导致Ag2CrO4沉淀过迟,影响实验结果 实验数据 实验数据实验序号 | FeSO4溶液体积读数/mL | |
| 滴定前 | 滴定后 | |
| 第一次 | 0.10 | 16.20 |
| 第二次 | 0.30 | 15.31 |
| 第三次 | 0.20 | 15.19 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c1>c2 | B.a1<a2 | C.碱性:甲<乙 | D.无法判断 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.配制标准溶液的固体NaOH中混有杂质KOH |
| B.滴定终点读数时,俯视滴定管的刻度,其他操作正确 |
| C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗 |
| D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×l0-10 | K1=4.3×10-7 K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.此时水的离子积KW=1×10-14 |
| B.水电离出的c(H+)=1×10-10mol·L-1 |
| C.水的电离程度随温度升高而增大 |
D.c(Na+)=c( ) ) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com