
【题目】HCN是一种剧毒性的酸,常温下,0.10molL-1HCN溶液的pH = 3,下列说法正确的是( )
A.HCN是一种强酸
B.相同浓度的NaCl溶液与NaCN溶液,前者的pH更大
C.在NaCN溶液中存在:c(Na+) = c(HCN) + c(CN-)
D.中和相同体积与浓度的HCl溶液与HCN溶液,所消耗的NaOH溶液的体积不同
【答案】C
【解析】
A选项,常温下,0.10molL-1 HCN溶液的pH = 3,即c(H+) =0.001molL-1,可知HCN不能完全电离,故为弱酸,故A错误;
B选项,NaCl是强碱强酸盐,不水解,溶液显中性,即pH = 7;而NaCN为强碱弱酸盐,水解显碱性,pH大于7,故相同浓度的NaCl溶液与NaCN溶液,后者的pH更大,故B错误;
C选项,在NaCN溶液中,![]() 是弱酸根,在溶液中能部分水解为HCN分子,根据物料守恒可知,c(Na+) = c(HCN) + c(CN-),故C正确;
是弱酸根,在溶液中能部分水解为HCN分子,根据物料守恒可知,c(Na+) = c(HCN) + c(CN-),故C正确;
D选项,相同体积与浓度的HCl溶液与HCN溶液中HCl与HCN的物质的量相同,且两者均为一元酸,故消耗的氢氧化钠的体积相同,故D错误。
综上所述,答案为C。


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】华法林(Warfarin )又名杀鼠灵,为心血管疾病的临床药物。其合成路线(部分反应条件略去)如图所示

回答下列问题
⑴A的名称为______,F中官能团名称为________、________。
⑵B的结构简式为_____。③的反应类型为_____,⑧的反应类型为_____。
⑶在一定条件下l mol 的华法林最多反应_______molH2
⑷写出由C 生成 D 的化学方程式为 ___________;
⑸F的同分异构体甚多,满足下列条件:①属芳香族化合物②发生银镜反应③和NaOH溶液反应,共___种,其中遇氯化铁显紫色且苯环上的一氯代物只有两种结构的结构简式_________。
⑹若D为乙醛,按框图中④同样的反应物和条件,写出生成物的结构简式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B两元素的最外层都只有一个电子,A的原子序数等于B的原子序数的11倍,A离子的电子层结构与周期表中非金属性最强的元素的阴离子的电子层结构相同;元素C与B易形成化合物B2C,该化合物常温下呈液态,则:
(1)A的原子结构示意图为____,在固态时属于___晶体。
(2)C的单质属于___晶体。B与C形成化合物B2C的化学式为___,电子式为____;它是由___键形成的___分子,在固态时属于___晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某溶液中由水电离出的c(H+)和c(OH-)的乘积是1×10-20,下列说法中正确的是( )
A.该溶液的溶质不可能是NaHCO3B.该溶液的pH一定是10
C.该溶液的溶质不可能是NaHSO4D.该溶液的溶质可能是正盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL0.1mol/L的某一元酸HR溶液中逐滴加入0.1mol/L氨水,所得溶液pH及导电能力变化如图。下列分析不正确的是( )
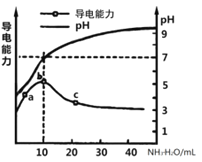
A. a~b点导电能力增强说明HR为弱酸
B. a、b点所示溶液中水的电离程度不相同
C. b恰好完全中和,pH=7说明NH4R没有水解
D. c 点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的表述正确的是( )
A.NH4Cl的水解常数表达式:![]()
B.NaHCO3水解的离子方程式:HCO3- + H2O ![]() H3O + + CO32-
H3O + + CO32-
C.结构示意图为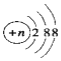 的阴离子都不能破坏水的电离平衡
的阴离子都不能破坏水的电离平衡
D.H2SO3的电离方程式:H2SO3![]() 2H+ + SO32-
2H+ + SO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A.FeS2![]() SO2
SO2![]() H2SO4
H2SO4
B.N2![]() NH3
NH3![]() NO
NO![]() NO2
NO2![]() HNO3
HNO3
C.Fe![]() FeCl2
FeCl2![]() FeCl3
FeCl3![]() Fe(OH)3
Fe(OH)3
D.MnO2![]() Cl2
Cl2![]() 漂白粉
漂白粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气在科研、生产中有广泛应用。
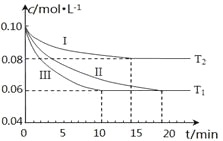
(1)在三个1L的恒容密闭容器中,分别加入0.1mol N2和0.3mol H2发生反应N2(g)+3H2(g)![]() 2NH3(g)ΔH1<0,实验Ⅰ、Ⅱ、Ⅲ中c(N2)随时间(t)的变化如图所示(T表示温度)。
2NH3(g)ΔH1<0,实验Ⅰ、Ⅱ、Ⅲ中c(N2)随时间(t)的变化如图所示(T表示温度)。
①实验Ⅲ在前10分钟内N2平均反应速率v(N2)=_________________________;(写出计算过程)
②与实验Ⅱ相比,实验Ⅰ、实验Ⅲ分别采用的实验条件可能为_____________、__________________。
(2)常温下NH4+(aq)+H2O(l)![]() NH3H2O(aq)+H+(aq)的化学平衡常数为5.55×10-10mol·L-1,则NH3H2O的电离平衡常数K=______________________(保留三位有效数字)。
NH3H2O(aq)+H+(aq)的化学平衡常数为5.55×10-10mol·L-1,则NH3H2O的电离平衡常数K=______________________(保留三位有效数字)。
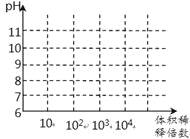
(3)常温下,将1mL pH均为11的氨水与NaOH溶液分别加水稀释,请在右图中画出两溶液的pH随体积稀释倍数的变化曲线______________(加必要标注)。
(4)工业上用NH3消除NO污染。在一定条件下,已知每还原1molNO,放出热量120kJ,请完成下列热化学方程式: NO(g)+ NH3(g)= N2(g)+______(g) ΔH2=__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是产生和收集气体的实验装置,该装置适合于( )
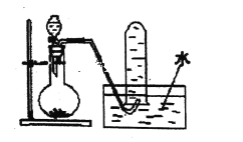
A.用浓硝酸与Cu反应制取NO2B.用浓盐酸和MnO2反应制取Cl2
C.用H2O2溶液和MnO2反应制取O2D.用NH4Cl和Ca (OH)2反应制取NH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com