
【题目】下列与金属腐蚀有关的说法,正确的是( )
A.图1中,插入海水中的铁棒,越靠近底端腐蚀越严重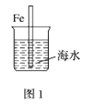
B.图2中,插入溶液中的铁棒容易溶解,主要是发生电化学腐蚀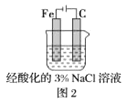
C.图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生电化学腐蚀
D.图4中,用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的负极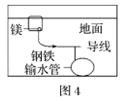
科目:高中化学 来源: 题型:
【题目】常温下,用0.1 mol·L-1NaOH溶液滴定20 mL 0.1 mol·L-1CH3COOH溶液的滴定曲线如图所示。下列说法正确的是

A. 点①所示溶液中:c(Na+)>c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)
B. 点②所示溶液中:c(Na+)+c(H+)=c(CH3COO-) +c(CH3COOH) +c(OH-)
C. 点③所示溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D. 在整个滴定过程中:溶液中![]() 始终不变
始终不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对伞花烃(a)常用作染料、医药、香料的中间体,a可转化为b(如图)。下列说法错误的是( )
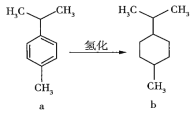
A.常温下对伞花烃呈液态且难溶于水
B.b物质的一氯代物有5种
C.对伞花烃分子中最多有9个碳原子共平面
D.图中氢化反应既是加成反应也是还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的有( )
A.第四周期元素中,锰原子价电子层中未成对电子数最多
B.第二周期主族元素的原子半径随核电荷数增大依次减小
C.卤素氢化物中,![]() 的沸点最低的原因是其分子间的范德华力最小
的沸点最低的原因是其分子间的范德华力最小
D.价层电子对互斥理论中,π键电子对数不计入中心原子的价层电子对数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列反应可用于检测司机是否酒后驾驶:![]()
![]() 。
。
①配合物![]() 中,与
中,与![]() 形成配位键的原子是__________(填元素符号)。
形成配位键的原子是__________(填元素符号)。
②![]() 中
中![]() 原子的杂化轨道类型是________;
原子的杂化轨道类型是________;![]()
![]() 含有
含有![]() 键的数目为_______。
键的数目为_______。
(2)![]() 分子中,
分子中,![]() 原子的杂化轨道类型是__________;写出由3个原子组成且与
原子的杂化轨道类型是__________;写出由3个原子组成且与![]() 具有相同空间构型的离子:___________(填一个即可)。
具有相同空间构型的离子:___________(填一个即可)。
(3)石墨烯(结构如图1所示)是一种由单层碳原子构成的具有平面结构的新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(结构如图2所示)。
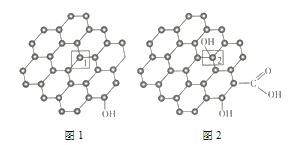
氧化石墨烯中2号![]() 原子的杂化方式是_________,该
原子的杂化方式是_________,该![]() 原子与相邻
原子与相邻![]() 原子形成的键角______(填“>”“<”或“=”)石墨烯中1号
原子形成的键角______(填“>”“<”或“=”)石墨烯中1号![]() 与相邻
与相邻![]() 形成的键角。
形成的键角。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是电解饱和 NaCl 溶液的实验装置,x、y 都是惰性电极,a 是饱和 NaCl 溶液,同时在两边各滴入几滴酚酞试液,下列有关该实验正确的说法是

A.x 电极为阳极,y 电极为阴极
B.x 电极附近溶液变红色,且有刺激性气味气体产生
C.若将两电极产生的气体收集起来,X电极得到的气体与Y电极得到的气体之比之比略大于 1:1
D.电解后,将溶液混匀,电解前后溶液的 pH 未发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K=___,ΔH___0(填“<”“>”或“=”)。
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003molL-1s-1,则6s时c(A)=___molL-1,C的物质的量为___mol;若反应经一段时间后,达到平衡时A的转化率为___,如果这时向该密闭容器中再充入1mol氩气,平衡时A的转化率为___。
(3)一定温度下,能判断该反应达化学平衡状态的是___。
①单位时间内生成nmolA,同时消耗nmolC
②A的转化率不变
③容器内压强不再变化
④混合气体的密度不再变化
⑤混合气体的平均相对分子质量不再变化
(4)1200℃时,C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为___。
A(g)+B(g)的平衡常数的值为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究高效催化剂是解决汽车尾气中的 NO 和 CO 对大气污染的重要途径。
(1)已知:C(s)+O2(g)=CO2(g) △H1=-393.5 kJ/mol
C(s)+![]() O2(g)= CO(g) △H2= -110.5 kJ/mol
O2(g)= CO(g) △H2= -110.5 kJ/mol
N2(g)+ O2(g)=2NO(g) △H3= +180.0 kJ/mol
则汽车尾气的催化转化反应 2NO(g)+ 2CO(g)=N2(g)+ 2CO2(g)的△H =_______kJ/mol。
(2)400℃时,在分别装有催化剂 A 和 B 的两个容积为 2 L 的刚性密闭容器中,各充入物质的量均为nmol的NO和CO发生上述反应。通过测定容器内总压强随时间变化来探究催化剂对反应速率的影响,数据如下表:
时间/min | 0 | 10 | 20 | 30 | ∞ |
A容器内压强/kPa | 75.0 | 70.0 | 65.0 | 60.0 | 60.0 |
B容器内压强/kPa | 75.0 | 71.0 | 68.0 | 66.0 | 60.0 |
①由上表可以判断催化剂 __________(填“A”或“B”) 的效果更好。
②容器中CO 的平衡转化率为 __________。400℃时,用压强表示的平衡常数Kp__________(kPa)-1 (保留两位小数)。
③汽车尾气排气管中使用催化剂可以提高污染物转化率,其原因是 __________。
(3)为研究气缸中NO的生成, 在体积可变的恒压密闭容器中,高温下充入物质的量均为 1mol 的氮气和氧气,发生反应 N2(g)+ O2(g)2NO(g)。
①下列说法能表明该反应已经达到平衡状态的是_________(填序号)。
A.2v正(O2)= v逆(NO) B.混合气体的平均相对分子质量不变
C.c(N2):c(O2)=l D.容器内温度不变
②为减小平衡混合气中 NO 的体积分数, 可采取的措施是 ___________。
(4)对于缸中NO的生成,化学家提出了如下反应历程:
第一步 O22O 慢反应
第二步 O+N2NO+N 较快平衡
第三步 N+O2NO+O 快速平衡
下列说法错误的是_______(填标号)。
A.第一步反应不从N2分解开始,是因为N2比O2稳定
B.N、O 原子均为该反应的催化剂
C.三步反应中第一步反应活化能最大
D.三步反应的速率都随温度升高而增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com