
下表中的实线表示元素周期表的部分过界。①~⑤分别表示元素周期表中对应位置的元素。

(1)元素③在周期表中的位置是 周期 族。
(2)元素③④⑤氢化物的稳定性由强到弱的顺序是 (用氢化物的化学式表示)。
(3)请在上表中用实线补全元素周期表边界。
(4)甲、乙两种化合物均由①②③④四种元素组成,写出此两种化合物在水溶液中发生反应的离子方程式 。
(5)X、Y、Z、W代表原子序数依次增大的四种短周期元素。在周期表中,Y与X相邻,Y与Z也相邻;X、Y和Z三种元素原子的最外层电子数之和为17;元素W与②形成离子化合物丙,物质丙的电子式为 ,写出实验室制W2的化学方程式,并标出电子转移的方向和数目: 。 X单质和①单质在一定条件下可生成化合物E(分子中有10个电子),分子的结构呈 ,晶体类型为 。
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
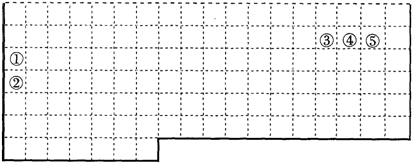
查看答案和解析>>
科目:高中化学 来源: 题型:
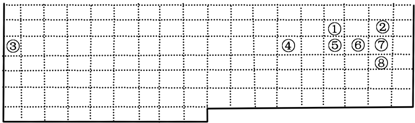
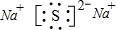
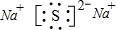
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | |||||||||||||||||
| ③ | ④ | ⑤ | |||||||||||||||
| ② | ⑥ | ⑧ | |||||||||||||||
| ⑦ | |||||||||||||||||
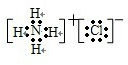
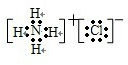
查看答案和解析>>
科目:高中化学 来源: 题型:
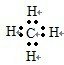
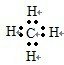
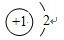 ;
;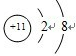
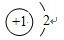 ;
;
查看答案和解析>>
科目:高中化学 来源:2013届浙江省高一下学期第一次质量检测化学试卷 题型:填空题
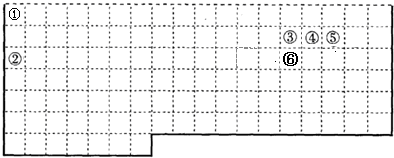
(10分)下表中的实线表示元素周期表的部分边界。①-⑥分别表示元素周期表中对应位置的元素。
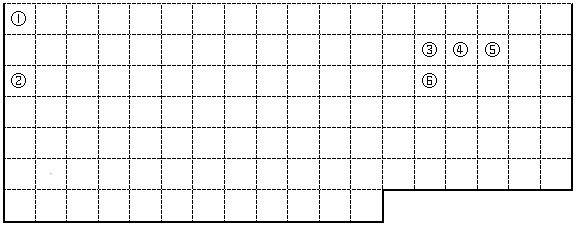
(1)请在表中用粗实线补全元素周期表边界。
(2)②号元素位于第 周期 族。
(3)写出由①、③两种元素组成的摩尔质量最小的化合物的电子式 ,上述元素中能和⑤号元素形成的原子晶体的化学式是
(4)上述元素中的一种元素其气态氢化物和该元素的最高价氧化物的水化物能发生化合反应,该反应的化学反应方程式为_____________,该生成物质含有的化学键类型是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com