
| A£®Ó¦ÓĆøĒĖ¹¶ØĀÉ£¬æɼĘĖćijŠ©ÄŃŅŌÖ±½Ó²āĮæµÄ·“Ó¦ģŹ±ä |
| B£®1 mol SĶźČ«Č¼ÉÕ·ÅČČ297.3 kJ£¬ĘäČČ»Æѧ·½³ĢŹ½£ŗS£«O2=SO2””¦¤H£½£297.3 kJ”¤mol£1 |
| C£®1 mol H2SO4Óė1 mol Ba£ØOH£©2·“Ӧɜ³É1 mol BaSO4³ĮµķŹ±·Å³öµÄČČĮ潊×öÖŠŗĶČČ |
| D£®·“Ó¦ČȵēóŠ”Óė·“Ó¦ĪļĖł¾ßÓŠµÄÄÜĮæŗĶÉś³ÉĪļĖł¾ßÓŠµÄÄÜĮæĪŽ¹Ų |
 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®“ųĻą·“µēŗɵĥė×ÓÖ®¼äµÄĻą»„ĪüŅżĮ¦³ĘĪŖĄė×Ó¼ü |
| B£®½šŹōŌŖĖŲÓė·Ē½šŹōŌŖĖŲ»ÆŗĻŹ±£¬²»Ņ»¶ØŠĪ³ÉĄė×Ó¼ü |
| C£®Ä³ŌŖĖŲµÄŌ×Ó×īĶā²ćÖ»ÓŠŅ»øöµē×Ó£¬ĖüÓėĀ±ĖŲ½įŗĻŹ±ĖłŠĪ³ÉµÄ»Æѧ¼ü²»Ņ»¶ØŹĒĄė×Ó¼ü |
| D£®·Ē½šŹōŌŖĖŲŅ²æÉÄÜŠĪ³ÉĄė×Ó¼ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
A£®ŅŃÖŖ2H2(g)+O2(g) 2H2O(g)””¦¤H="-483.6" kJ/mol,ŌņĒāĘųµÄČ¼ÉÕČČĪŖ241.8 kJ 2H2O(g)””¦¤H="-483.6" kJ/mol,ŌņĒāĘųµÄČ¼ÉÕČČĪŖ241.8 kJ |
B£®ÓÉC(ŹÆÄ«,s) C(½šøÕŹÆ,s)””¦¤H="+11.9" kJ”¤mol-1æÉÖŖ,½šøÕŹÆ±ČŹÆÄ«ĪČ¶Ø C(½šøÕŹÆ,s)””¦¤H="+11.9" kJ”¤mol-1æÉÖŖ,½šøÕŹÆ±ČŹÆÄ«ĪČ¶Ø |
C£®Ķ¬ĪĀĶ¬Ń¹ĻĀ,H2(g)+Cl2(g) 2HCl(g)ŌŚ¹āÕÕŗĶµćČ¼Ģõ¼žµÄ¦¤H²»Ķ¬ 2HCl(g)ŌŚ¹āÕÕŗĶµćČ¼Ģõ¼žµÄ¦¤H²»Ķ¬ |
| D£®ČĪŗĪŅ»øö»Æѧ±ä»Æ¶¼°éĖę×ÅÄÜĮæµÄ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
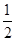 O2£Øg£©=CO2£Øg£©£«2H2£Øg£©
O2£Øg£©=CO2£Øg£©£«2H2£Øg£©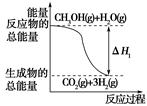
| A£®·“Ó¦¢ŁÖŠµÄÄÜĮæ±ä»ÆČēÉĻĶ¼ĖłŹ¾ |
| B£®CH3OH×Ŗ±ä³ÉH2µÄ¹ż³ĢŅ»¶ØŅŖĪüŹÕÄÜĮæ |
| C£®1 mol CH3OH³ä·ÖČ¼ÉշųöµÄČČĮæĪŖ192.9 kJ |
| D£®æÉĶĘÖŖ2H2£Øg£©£«O2£Øg£©=2H2O£Øg£© ¦¤H£½£483.8 kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
A£®C(s)£« O2(g)=CO(g)¦¤H£½£393.5 kJ/mol O2(g)=CO(g)¦¤H£½£393.5 kJ/mol |
| B£®2H2(g)£«O2(g)=2H2O(l)¦¤H£½£571.6 kJ/mol |
| C£®CH4(g)£«2O2(g)=CO2(g)£«2H2O(g)¦¤H£½£890.3 kJ/mol |
D£® C6H12O6(s)£«3O2(g)=3CO2(g)£«3H2O(g)¦¤H£½£1 400 kJ/mol C6H12O6(s)£«3O2(g)=3CO2(g)£«3H2O(g)¦¤H£½£1 400 kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā

 2CO£«O2””¢Ś2H2O===2H2£«O2””¢Ū2N2£«6H2O
2CO£«O2””¢Ś2H2O===2H2£«O2””¢Ū2N2£«6H2O 4NH3£«3O2””¢Ü2CO2£«4H2O
4NH3£«3O2””¢Ü2CO2£«4H2O 2CH3OH£«3O2””¢Ż2CO£«4H2O
2CH3OH£«3O2””¢Ż2CO£«4H2O ________£«3O2
________£«3O2| ¹²¼Ū¼ü | H”ŖN | H”ŖO | N”ŌN | O===O |
| ¶ĻĮŃ1 mol»Æѧ¼üĖłŠčÄÜĮæ/(kJ”¤mol£1) | 393 | 460 | 941 | 499 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
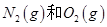 ·“Ӧɜ³É
·“Ӧɜ³É ¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®Ķس£ĒéæöĻĀ£¬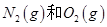 »ģŗĻÄÜÖ±½ÓÉś³ÉNO »ģŗĻÄÜÖ±½ÓÉś³ÉNO |
B£®1mol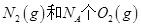 ·“Ó¦·Å³öµÄÄÜĮæĪŖ180kJ ·“Ó¦·Å³öµÄÄÜĮæĪŖ180kJ |
| C£®NOŹĒŅ»ÖÖĖįŠŌŃõ»ÆĪļ£¬ÄÜÓėNaOHČÜŅŗ·“Ӧɜ³ÉŃĪŗĶĖ® |
D£®1mol ¾ßÓŠµÄ×ÜÄÜĮæŠ”ÓŚ2mol ¾ßÓŠµÄ×ÜÄÜĮæŠ”ÓŚ2mol  ¾ßÓŠµÄ×ÜÄÜĮæ ¾ßÓŠµÄ×ÜÄÜĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
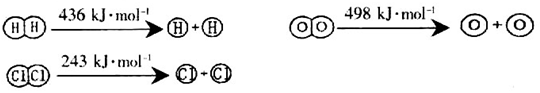
 ,ĖüĖł¶ŌÓ¦µÄ»Æѧ·½³ĢŹ½ĪŖ________________”£
,ĖüĖł¶ŌÓ¦µÄ»Æѧ·½³ĢŹ½ĪŖ________________”£ 2NH3(g) ”÷H£¼0ŌŚ400”ꏱK£½0.5£¬“ĖĢõ¼žĻĀŌŚ0.5LµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠøĆ·“Ó¦£¬Ņ»¶ĪŹ±¼äŗ󣬲āµĆN2”¢H2”¢NH3µÄĪļÖŹµÄĮæ·Ö±šĪŖ2mol”¢1mol”¢2mol£¬Ōņ“ĖŹ±·“Ó¦¦Ō(N2)Õż______¦Ō(N2)Äę£ØĢī”°£¾”±”¢”°£¼”±»ņ”°£½”±£©”£ÓūŹ¹µĆøĆ·“Ó¦µÄ»Æѧ·“Ó¦ĖŁĀŹ¼Óæģ£¬Ķ¬Ź±Ź¹Ę½ŗāŹ±NH3µÄĢå»ż°Ł·ÖŹżŌö¼Ó£¬æɲÉČ”µÄ“ėŹ©ŹĒ_______£ØĢīŠņŗÅ£©”£
2NH3(g) ”÷H£¼0ŌŚ400”ꏱK£½0.5£¬“ĖĢõ¼žĻĀŌŚ0.5LµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠøĆ·“Ó¦£¬Ņ»¶ĪŹ±¼äŗ󣬲āµĆN2”¢H2”¢NH3µÄĪļÖŹµÄĮæ·Ö±šĪŖ2mol”¢1mol”¢2mol£¬Ōņ“ĖŹ±·“Ó¦¦Ō(N2)Õż______¦Ō(N2)Äę£ØĢī”°£¾”±”¢”°£¼”±»ņ”°£½”±£©”£ÓūŹ¹µĆøĆ·“Ó¦µÄ»Æѧ·“Ó¦ĖŁĀŹ¼Óæģ£¬Ķ¬Ź±Ź¹Ę½ŗāŹ±NH3µÄĢå»ż°Ł·ÖŹżŌö¼Ó£¬æɲÉČ”µÄ“ėŹ©ŹĒ_______£ØĢīŠņŗÅ£©”£ 2C(g)£«D(s) ”÷H£¬Ęä»ÆŃ§Ę½ŗā³£ŹżKÓėTµÄ¹ŲĻµČēĻĀ±ķ£ŗ
2C(g)£«D(s) ”÷H£¬Ęä»ÆŃ§Ę½ŗā³£ŹżKÓėTµÄ¹ŲĻµČēĻĀ±ķ£ŗ| T/K | 300 | 400 | 500 | ”” |
| K/(mol”¤L£1)2 | 4”Į106 | 8”Į107 | 1.2”Į109 | ”” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®µČÖŹĮæµÄĮņÕōĘųŗĶĮņ¹ĢĢå·Ö±šĶźČ«Č¼ÉÕ£¬ŗóÕ߷ųöµÄČČĮæ¶ą |
B£®ÓÉC£ØŹÆÄ«£© C£Ø½šøÕŹÆ£© ¦¤H="+1.9" KJ/molæÉÖŖ£¬½šøÕŹÆ±ČŹÆÄ«ĪČ¶Ø C£Ø½šøÕŹÆ£© ¦¤H="+1.9" KJ/molæÉÖŖ£¬½šøÕŹÆ±ČŹÆÄ«ĪČ¶Ø |
| C£®1mol H2ŌŚ×ćĮæCl2ÖŠČ¼ÉÕ·ÅČČ183KJ£¬ŌņH2µÄČ¼ÉÕČČĪŖ183KJ”£ |
| D£®ŌŚĻ”ČÜŅŗÖŠ£¬H+(aq)+OH-(aq)==H2O(l)¦¤H="-57.3" kJ/mol,Čō½«ŗ¬0.5 mol H2SO4µÄÅØĮņĖįÓėŗ¬1 mol NaOHµÄČÜŅŗ»ģŗĻ£¬Õūøö¹ż³Ģ·Å³öµÄČČĮæ“óÓŚ57.3 kJ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com