
| A. | 某温度下,pH=7的NH4Cl与NH3•H2O的混合溶液:c(NH4+)=c(Cl-)>c(H+)=c(OH-) | |
| B. | 0.1 mol/L Na2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| C. | 25℃时,pH=2的HCOOH与pH=12的NaOH等体积混合:c(HCOO-)<c(Na+) | |
| D. | 0.1 mol/L Na2CO3溶液与0.1 mol/L NaHCO3溶液等体积混合:3c(CO32-)+3c(HCO3-)+3c(H2CO3)=2c(Na+) |
分析 A.某温度下溶液PH=7溶液不一定为中性;
B.硫化钠溶液中存在质子守恒,水电离出的所有氢氧根离子浓度等于所有氢离子存在形式的离子浓度;
C.甲酸中存在电离平衡,反应后继续电离生成甲酸根离子和氢离子,溶液显酸性;
D.溶液中存在物料守恒,2n(Na)=3n(C).
解答 解:A.常温下,混合溶液中pH=7不能说明溶液呈中性,溶液中存在电荷守恒得C(H+)+C(NH4+)=C(OH-)+C(Cl-),但不一定存在c(NH4+)=c(Cl-)>c(H+)=c(OH-),故A错误;
B.0.1mol/LNa2S溶液中硫离子水解结合氢离子,水电离出的所有氢氧根离子浓度和氢离子浓度相同:c(OH-)=c(H+)+c(HS-)+2c(H2S),故B错误;
C.25℃时,pH=2的HCOOH与pH=12的NaOH等体积混合,甲酸平衡状态下氢离子和氢氧根离子恰好反应,甲酸又电离出甲酸根离子和氢离子,溶液呈酸性,c(HCOO-)>c(Na+),故C错误;
D.0.1mol/LNa2CO3溶液与0.1mol/L NaHCO3溶液等体积混合,依据物料守恒:3c(CO32-)+3c(HCO3-)+3c(H2CO3)=2c(Na+),故D正确;
故选D.
点评 本题考查了电解质溶液中的离子浓度比较,电荷守恒,质子守恒,物料守恒的分析判断,题目难度中等.


科目:高中化学 来源: 题型:选择题
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 0.60 | 0.30 |
| t1 | 0.40 | |
| t2 | 0.10 |
| A. | 反应在t1min内的平均速率为v(H2)=0.20/t1mol•L-1•min-1 | |
| B. | 保持其他条件不变,向平衡体系中再通入0.10molH2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数减小 | |
| C. | 温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应 | |
| D. | 700℃时,若向密闭容器中充入CO(g)、H2O(g)、CO2(g)、H2(g)的物质的量分别为0.60mol、1.00mol、0.60mol、0.60mol,则此时该反应v(正)<v(逆) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
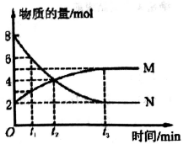 一定温度下,在体积为2L的密闭容器中通入气体M和N并发生反应,物质的量随时间的变化关系如图.下列说法正确的是( )
一定温度下,在体积为2L的密闭容器中通入气体M和N并发生反应,物质的量随时间的变化关系如图.下列说法正确的是( )| A. | M、N之间转化的反应方程式为M=2N | |
| B. | t2时刻,反应达到平衡,正、逆反应速率达到相等 | |
| C. | t3时刻,M的反应速率为$\frac{3}{2{t}_{3}}$mol•L-1•min-l | |
| D. | t1时刻,在容器内气体M和N的物质的量浓度之比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下用二氧化锰和浓盐酸反应制取Cl2 | |
| B. | 用饱和氯化钠溶液可以洗涤除去氯化钠固体表面少量氯化钾杂质 | |
| C. | 向某溶液中加入盐酸酸化的BaCl2溶液,产生白色沉淀,可知该溶液中一定含有SO42- | |
| D. | 向浓度均为0.01mol/L的K2SO4和KI混合溶液中滴加Pb(NO3)2溶液,先生成PbI2黄色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 恒温恒容时,充入CO气体,达到新平衡时$\frac{c(C{O}_{2})}{c(CO)}$增大 | |
| B. | 容积不变时,升高温度,混合气体的平均相对分子质量减小 | |
| C. | 恒温恒容时,分离出部分SO2气体可提高MgSO4的转化率 | |
| D. | 恒温时,增大压强平衡逆向移动,平衡常数减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜跟稀HNO3反应:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| B. | 向硫酸铝溶液中加入过量氨水:Al3++3OH-═AlO2-+2H2O | |
| C. | 向Ag(NH3)2NO3溶液中加入盐酸:Ag(NH3)2+2H+═Ag++2NH4+ | |
| D. | NaHSO4溶液和Ba(OH)2溶液混合后溶液呈中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
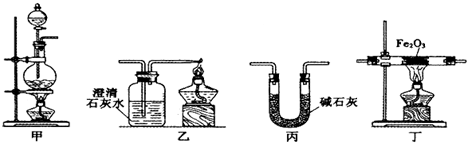
| 加热方式 | 通CO加热 时间/min | 澄清石灰水变 浑浊时间/min | 产物颜色 | 产物能否全部 被磁铁吸引 |
| 酒精灯 | 30 | 5 | 黑色 | 能 |
| 酒精喷灯 | 30 | 1 | 黑色 | 能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCL(aq)$\stackrel{CO_{2}}{→}$NaHCO3(s)$\stackrel{△}{→}$NaCO3(s) | |
| B. | FeSz$→_{燃烧}^{O_{2}}$SO2$\stackrel{H_{2}O}{→}$H2SO4 | |
| C. | SiO2$\stackrel{HCl(aq)}{→}$SiCl4$→_{高温}^{H_{2}}$Si | |
| D. | N2$→_{高温、高压、催化剂}^{H_{2}}$NH3$\stackrel{HCl(aq)}{→}$NH4Cl(aq) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com