
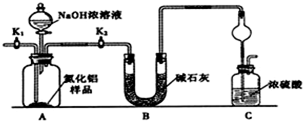
分析 (1)分析装置和仪器作用分析,氨气是和浓硫酸能发生反应的气体,易发生倒吸,仪器作用是防止倒吸的作用;
(2)组装好实验装置,依据原理可知气体制备需要先检查装置气密性,加入实验药品.接下来的实验操作是关闭K1,打开K2,反应生成氨气后卫把装置中的气体全部赶入装置C被浓硫酸吸收,准确测定装置C的增重计算;
(3)装置存在缺陷是空气中的水蒸气和二氧化碳也可以进入装置C,使测定结果偏高,需要连接一个盛碱石灰干燥管;
(4)依据氨气极易溶于水的性质分析判断;
(5)依据化学方程式定量关系计算得到,若m g样品完全反应,测得生成气体的体积为V mL(已转换为标准状况),
AIN+NaOH+H2O═NaAIO2+NH3↑
41 22.4L
m V×10-3L
m=$\frac{41V×1{0}^{-3}}{22.4}$,计算得到质量分数表达式;
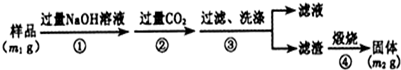
(6)步骤②生成的沉淀是氢氧化铝,是偏铝酸钠溶液中通入过量二氧化碳气体反应生成;
(7)沉淀不洗涤得到滤渣质量会增大,测定结果会偏高.
解答 解:(1)分析装置和仪器作用分析,氨气是与浓硫酸能发生反应的气体,易发生倒吸,图C装置中球形干燥管的作用是防止倒吸的作用,
故答案为:防止倒吸;
(2)组装好实验装置,原理可知气体制备需要先检查装置气密性,加入实验药品.接下来的实验操作是关闭K1,打开K2,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体.打开K1,通入氮气一段时间,测定C装置反应前后的质量变化.通入氮气的目的是,反应生成氨气后卫把装置中的气体全部赶入装置C被浓硫酸吸收,准确测定装置C的增重计算,
故答案为:检查装置气密性,把装置中残留的氨气全部赶入C装置;
(3)装置存在缺陷是空气中的水蒸气和二氧化碳也可以进入装置C,使测定结果偏高,需要连接一个盛碱石灰干燥管,
故答案为:C装置出口处连接一个干燥装置;
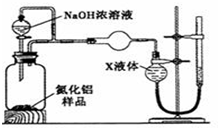
(4)依据氨气极易溶于水的性质分析,为测定生成气体的体积,量气装置中的X液体可以是;
A.CCl4不能溶解氨气,可以用排四氯化碳溶液的方法测定氨气体积,故A正确;
B.氨气极易溶于水,不能排水法测定,故B错误;
C.氨气极易溶于水,不能用排NH4Cl溶液的方法测定气体体积,故C错误;
D.氨气不溶于苯,可以利用排苯溶液,测定氨气的体积,故D正确;
故选AD;
(5)若m g样品完全反应,测得生成气体的体积为V mL(已转换为标准状况),
AIN+NaOH+H2O═NaAIO2+NH3↑
41 22.4L
m V×10-3L
m=$\frac{41V×1{0}^{-3}}{22.4}$
则AlN的质量分数=$\frac{4V×1{0}^{-3}}{22.4m}$×100%=$\frac{41V}{22400m}$×100%,
故答案为:$\frac{41V}{22400m}$×100%;
(6)步骤②生成的沉淀是氢氧化铝,是偏铝酸钠溶液中通入过量二氧化碳气体反应生成,反应的离子方程式为:CO2+AlO2-+2H2O=HCO3-+Al(OH)3↓,
故答案为:CO2+AlO2-+2H2O=HCO3-+Al(OH)3↓;
(7)若在步骤③中未洗涤,沉淀不洗涤得到滤渣质量会增大,测定结果会偏高,故答案为:偏高.
点评 本题考查了物质性质的探究实验设计和实验分析判断,实验基本操作和我物质性质的掌握是关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Na2S溶液显碱性:S2-+2H2O?H2S+2OH- | |
| B. | 用排饱和食盐水法收集Cl2:Cl2+H2O?H++Cl-+HClO | |
| C. | 草酸溶液使高锰酸钾酸性溶液褪色:2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O | |
| D. | 向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H2O?Al(OH)3(胶体)+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4++2H2O?NH3•H2O+H3O+ | B. | HCO3-+H2O?H3O++CO32- | ||
| C. | HS-+H+═H2S | D. | Cl2+H2O?H++Cl-+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
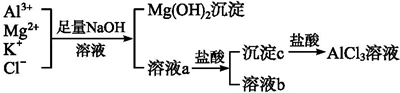
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 石油主要是各种烷烃、环烷烃、烯烃组成的混合物 | |
| B. | 做衣服的棉和麻均与淀粉互为同分异构体 | |
| C. | 煎炸食物的花生油和牛油都是可皂化的酯类 | |
| D. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | c(H+)•c(OH-)=10-14 | B. | c(Na+)+c(K+)=c(HA-)+2c(A2-) | ||
| C. | c(Na+)>c(K+) | D. | c(Na+)+c(K+)=0.05mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
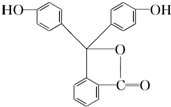 酚酞是中学化学中常用的酸碱指示剂,其结构如下,完成下列问题:
酚酞是中学化学中常用的酸碱指示剂,其结构如下,完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤干馏后的产物可以制造氮肥 | |
| B. | 可在周期表的过渡元素中寻找半导体材料 | |
| C. | 可用新制的氢氧化铜检验葡萄糖 | |
| D. | 可用氯气制备漂白粉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com