
在强酸性 溶液中能大量共存的无色透明离子组是( )
溶液中能大量共存的无色透明离子组是( )
A.K+、Na+、NO3-、MnO4- B.K+、Na+、Cl-、SO42-
C.K+、Na+、Br-、Cu2+ D.Na+、Ba2+、OH-、SO42-
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年西藏山南二中高二上学期期中化学试卷(解析版) 题型:选择题
下列反应中不属于可逆反应的是( )
A.2NO2 N2O4
N2O4
B.N2+3H2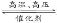 2NH3
2NH3
C.Cl2+H2O HCl+HClO
HCl+HClO
D.Pb+PbO2+2H2SO4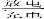 2PbSO4+2H2O
2PbSO4+2H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省六校协作体高一上期中化学试卷(解析版) 题型:选择题
①用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部
②给盛有液体的体积超过1/3容积的试管加热
③把鼻孔靠近容器口去闻气体的气味
④将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管
⑤取用放在细口瓶中的液体时,取下瓶塞倒放在桌面上,倾倒液体时,瓶上的标签对着地面
⑥将烧瓶放在桌上,用力塞紧塞子
⑦用坩埚钳夹取加热后的蒸发皿
⑧将滴管垂直伸进试管内滴加液体
⑨稀释浓硫酸时,把水迅速倒入盛有浓硫酸的量筒中
⑩检验装置的气密性时,把导管的一端浸入水中,用手捂住容器的外壁或用酒精灯微热
A. ①④⑦⑩ B. ①④⑤⑦⑩ C. ①④⑤⑦⑧⑩ D. ④⑤⑦⑩
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省六校协作体高一上期中化学试卷(解析版) 题型:选择题
已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:
H2O2→H2O;IO3-→I2;MnO4-→Mn2+;HNO2→NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
A.H2O2 B.IO3- C.MnO4- D.HNO2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省等六校高一上期中化学卷(解析版) 题型:实验题
A. 将配好的稀硫酸倒入试剂瓶中,贴好标签;
B. 盖好容量瓶塞,反复颠倒,摇匀;
C. 用量筒取 mL的18.0mol/L的浓硫酸;
D. 将 沿烧杯内壁慢慢注入盛有少量 的烧杯中;
E. 用少量蒸馏水洗涤烧杯2—3次,并将洗涤液也全部转移到容量瓶中;
F. 将已冷却至室温的硫酸溶液沿玻璃棒注入100mL的容量瓶中;
G. 改用胶头滴管逐滴加蒸馏水,使溶液凹面恰好与刻度相切;
H. 继续向容量瓶加蒸馏水,直到液面接近刻度线 cm处。
(1)填写上述步骤中的空白;
(2)请按正确的操作步骤进行排序 。
(3)试分析下列操作会使所配溶液的浓度会大于1.80mol/L浓度( )
A.用量筒取浓硫酸时,为了精确,用水洗涤量筒,并将洗涤液倒入烧杯中。
B.溶解后,立刻移液。
C.若加蒸馏水超过了刻度线,倒出一些溶液,再重新加蒸馏水到刻度线。
D.若定容时仰视看刻度线,会使稀硫酸溶液的浓度。
E.若摇匀后发现液面低于刻度线,又加水至刻度线。
(4)取20ml配好的硫酸,和足量的铝反应后,可收集到标准状况下的H2 ml.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省等六校高一上期中化学卷(解析版) 题型:选择题
某地甲、 乙两厂排放的污水中各含有下列8种离子中的4种(两厂废水所含离子不同):Ag+、Ba2+、Fe3+、Na+、C
乙两厂排放的污水中各含有下列8种离子中的4种(两厂废水所含离子不同):Ag+、Ba2+、Fe3+、Na+、C l-、SO
l-、SO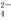 、NO
、NO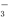 、OH-。若两厂单独排放污水都会造成严重的水污染,如将两厂的污水按一定比例混合,沉淀后污水便能变得无色澄清,溶质主要含硝酸钠,污染程度大大降低。根据所给信息有以下几种说法,你认为正确的是( )
、OH-。若两厂单独排放污水都会造成严重的水污染,如将两厂的污水按一定比例混合,沉淀后污水便能变得无色澄清,溶质主要含硝酸钠,污染程度大大降低。根据所给信息有以下几种说法,你认为正确的是( )
A.Na+和NO 可能来自同一工厂 B.Cl-和NO
可能来自同一工厂 B.Cl-和NO 一定来自同一工厂
一定来自同一工厂
C.Ag+和Na+可能来自同一工厂 D.SO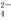 和OH-一
和OH-一 定来自同一
定来自同一 工厂
工厂
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省赣州市十四校高一上期中化学卷(解析版) 题型:填空题
某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+中的几种离子。
(1)不需做任何实验就可以肯定原溶液中不存在的离子是 。
(2)取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,原溶液中肯定有的离子是 ,发生反应的离子方程式为 。
(3)取(2)的滤液加入过量NaOH,出现白色沉淀,说明原溶液中肯定存在的离子有 。
(4)原溶液中不可能大量存在的阴离子是下列A~D中的(填序号) 。
A.Cl- B.NO3- C.CO32 - D.OH-
- D.OH-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省蕲春县高二上学期期中化学试卷(解析版) 题型:填空题
25 ℃,101 k Pa时,已知下列可逆反应的焓变和化学平衡常数分别为:
①A(g)+2B(g) 2C(g)+2D(l) ΔH1=-250.kJ·mol-1K1=0.2
2C(g)+2D(l) ΔH1=-250.kJ·mol-1K1=0.2
②E(s)+B(g) C(g) ΔH2=-310kJ·mol-1K2=2
C(g) ΔH2=-310kJ·mol-1K2=2
③F(g)+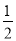 B(g)
B(g) D(l) ΔH3=-200kJ·mol-1K3=0.8
D(l) ΔH3=-200kJ·mol-1K3=0.8
(1)写出反应①的平衡常数表达式K1= ,升高反应①的温度,反应①的平衡常数 ,增大压强,反应①的平衡常数 (填“增大”或“减小”或“不变”)
(2)反应2F(g)+B(g) 2D(l) ΔH= ,反应②的逆反应的平衡常数K4=
2D(l) ΔH= ,反应②的逆反应的平衡常数K4=
(3)反应2E(s)+2F(g)+B(g) A(g)的ΔH= ,K=
A(g)的ΔH= ,K=
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com