
氮、硫、氯及其化合物是中学化学重要的组成部分.
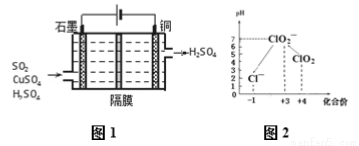
(1)氨气燃料电池使用的电解质溶液是 KOH 溶液,电池反应为:4NH3 +3O2 =2N2 +6H2O.该电池负极的电极反应式为___________;用该电池进行粗铜(含 Al、Zn、Ag、Pt、Au 等杂质)的电解精炼,以CuSO4溶液为电解质溶液,下列说法正确的是__________。
a.电能全部转化为化学能
b.SO42﹣的物质的量浓度不变(不考虑溶液体积变化)
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.若阳极质量减少64g,则转移电子数为2NA个
(2)已知KSP(BaSO 4)=1.0×10﹣10 ,KSP(BaCO3)=2.5×10﹣9 。
某同学设想用下列流程: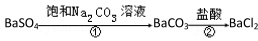 ,得到 BaCl2,则①的离子方程式为__________________,该反应的平衡常数K=__________;
,得到 BaCl2,则①的离子方程式为__________________,该反应的平衡常数K=__________;
科目:高中化学 来源:2016届湖北省高三5月模拟四理综化学试卷(解析版) 题型:选择题
茅台酒中存在少量具有凤梨香味的物质X,其结构如下图所示。下列说法正确的是
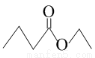
A.X难溶于乙醇
B.酒中的少量丁酸能抑制X的水解
C.分子式为C4H8O2且官能团与X相同的物质有5种
D.X完全燃烧后生成CO2和H2O的物质的量比为1∶2
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三全真模拟理综化学试卷(解析版) 题型:填空题
【化学选修3:物质结构与性质】Ⅰ.80%左右的非金属元素在现代技术包括能源、功能材料等领域占有极为重要的地位。
(1)氮及其化合物与人类生产、生活息息相关,基态N原子中电子在2p轨道上的排布遵循的原则是__________,N2F2分子中N原子的杂化方式是_____________,1mol N2F2含有___________个σ键.
(2)高温陶瓷材料Si3N4晶体中键角N-Si-N___Si-N-Si(填“>”“<”或“=”),原因是__________;
II.金属元素在现代工业中也占据极其重要的地位,钛也被称为“未来的钢铁”,具有质轻,抗腐蚀,硬度大,是宇航、航海、化工设备等的理想材料。
(4)基态钛原子核外共有________种运动状态不相同的电子.金属钛晶胞如下图1所示,为_______堆积(填堆积方式).

(5)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图2.化合物乙的沸点明显高于化合物甲,主要原因是_____________;化合物乙中采取sp3杂化的原子的电负性由大到小的顺序为_____________;
(6)钙钛矿晶体的结构如图3所示.假设把氧离子看做硬球接触模型,钙离子和钛离子填充氧离子的空隙,氧离子形成正八面体,钛离子位于正八面体中心,则一个钛离子被________个氧离子包围。
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三考前热身理综化学试卷(解析版) 题型:填空题
难溶性杂卤石(K2SO4·MgSO4·2CaSO4·2H2O)属于“呆矿”,在水中存在如下平衡
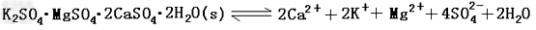
为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如下:
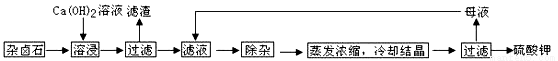
(1)滤渣主要成分有_______和_______以及未溶杂卤石。
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:
____ 。
(3)“除杂”环节中,先加入_______溶液,经搅拌等操作后,过滤,再加入_______溶液调滤液PH至中性。
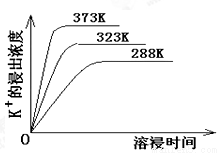
(4)不同温度下,K+的浸出浓度与溶浸时间的关系如下图,由图可得,随着温度升高,
①________________________②_______________
(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:
 已知298K时,Ksp(CaCO3)
已知298K时,Ksp(CaCO3)
=2.80×10-9,Ksp(CaSO4)=4.90×10-5,则此温度下该反应的平衡常数K为
(计算结果保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三考前热身理综化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.红宝石、玛瑙、水晶、钻石等装饰品的主要成分都不相同
B.将Al2(SO4)3溶液蒸干、灼烧至恒重,最终剩余固体是Al2O3
C.白磷、臭氧、碳—60、氩、水等物质都是由分子构成的,分子内都存在共价键
D.工业生产玻璃、水泥、漂白粉,均需要用石灰石为原料
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前模拟理综化学试卷(解析版) 题型:选择题
下列反应的离子方程式正确的是( )
A.向硫酸铝溶液中加入少量的氨水:Al3++3OH-=Al(OH) 3↓
B.向碳酸钠溶液中加入饱和石灰水:Ca(OH)2 +CO32-=CaCO3↓+2OH-
C.向氢氧化钠溶液中通入过量的氯气:Cl2+2OH-=ClO-+Cl-+H2O
D.向稀硫酸中加入过量铁粉,先后发生两个反应:2Fe+6H+=2Fe3+ +3H2↑,Fe+2Fe3+=3Fe2+
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前模拟理综化学试卷(解析版) 题型:选择题
设 N A 表示阿伏加德罗常数,下列说法中正确的是( )
A.标准状况下,l L 甲醇完全燃烧后生成的 CO 2 分子个数约为(1/22.4)N A
B.N A个H 2分子的质量约为2g,它所占的体积约为 22.4L
C.标准状况下,22.4L CO2与CO的混合气体中含有的碳原子数为N A
D.500mL 0.5mol/L 的Ca(ClO)2溶液中,含有ClO-的数目为0.5NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二6月月考化学试卷(解析版) 题型:选择题
取两份质量相等的有机物M,一份与足量的钠反应放出气体V1L,另一份与足量NaHCO3溶液反应放出气体V2L;若同温同压下V1=V2,则M是
A.HCOOH
B.HOOC—COOH
C.HOCH2CH2COOH
D.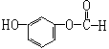
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古赤峰二中高二6月月考化学试卷(解析版) 题型:选择题
向CuSO4溶液中逐滴加入过量KI溶液,观察到产生白色沉淀,溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色.则下列分析中正确的是( )
A.白色沉淀是CuI2,棕色溶液含有I2
B.滴加KI溶液时,转移1 mol电子时生成1 mol白色沉淀
C.通入SO2时,SO2与I2反应,I2作还原剂
D.上述实验条件下,物质的氧化性:Cu2+>SO2>I2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com